Impact économique des perturbateurs endocriniens en Europe
Contexte
Dans le cadre du programme REACH (Registration, Evaluation, Authorization and restriction of Chemicals), la Commission européenne (CE) travaille activement à l’implantation, sur son territoire, d’une réglementation visant à encadrer la production et l’usage des agents chimiques considérés comme « perturbateurs endocriniens » (PE). Un PE est défini par la CE comme étant une « substance exogène causant un effet néfaste chez un organisme sain, ou sa progéniture, par l’entremise de changements dans la fonction endocrinienne ».
Ce projet de réglementation, qui vise notamment la classification de ces substances pour baliser leur autorisation, restriction, retrait progressif ou bannissement, est particulièrement important dans le contexte des politiques publiques de santé environnementale liées à la gestion des risques associés aux produits chimiques. En effet, il est susceptible de créer un précédent scientifique et réglementaire pour les pays cherchant à se conformer aux conventions internationales, telles que la SAICM (Strategic Approach to International Chemicals Management).
Parmi les éléments de gestion de risques à considérer, la CE a demandé aux auteurs de l’article dont il est question ici d’évaluer les coûts directs et indirects pouvant être associés au fardeau de maladies attribuables à l’exposition humaine au PE en Europe (Trasande et al., 2015). Plus spécifiquement, l’étude visait à :
- Estimer la nature et l’impact des maladies et des incapacités attribuables aux PE;
- Évaluer la probabilité de causalité entre l’exposition et les problèmes qui en découlent;
- Quantifier les coûts attribuables aux PE.
Méthodologie
Le calcul par les auteurs des coûts de santé attribués aux PE repose sur la détermination, commune en épidémiologie environnementale, de la fraction attribuable (FA) :
Équation 1
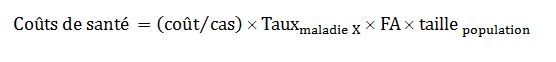
D’après les auteurs, la FA est définie comme étant « le pourcentage d’une catégorie de maladie qui serait éliminé si les facteurs de risque environnementaux étaient réduits à leurs plus faibles concentrations possibles » (Smith et al., 1999, cité dans Trasande et al., 2015). Les distributions statistiques de valeurs possibles que peut prendre la variable probabiliste « coût/cas » pour chacun des problèmes de santé examinés étaient tirées de lignes directrices bien établies en la matière.
Lors du calcul de coûts selon l’équation 1, ces distributions ont été prises en compte par l’approche de simulations de Monte-Carlo; les coûts totaux incluent à la fois les coûts directs associés au traitement et à la prise en charge des cas, ainsi que les coûts indirects découlant du manque à gagner « sociétal », par exemple, la perte de productivité économique. Les auteurs soulignent que l’évaluation ne couvre pas l’ensemble des coûts indirects et intangibles comme ceux de nature psychologique, mais ils ne détaillent pas davantage ce type de coûts.
L’exercice général est donc relativement simple en termes de calculs, quoique les auteurs ne précisent pas si le « taux de maladie » est un taux de prévalence ou d’incidence, et utilisent de manière apparemment indiscernable les deux termes dans l’article.
Le principal problème est d’évaluer la FA pour chaque maladie associée à un PE. À cette fin, Trasande et al. (2015) ont examiné la relation entre neuf substances – ou groupes de substances –, dont le polybromodiphényléther (PBDE), les pesticides organophosphorés (OP), le dichlorodiphényldichloroéthylène (DDE), le bisphénol A (BPA) et divers phtalates, et dix effets sanitaires néfastes ou des maladies, incluant la perte de quotient intellectuel (QI), l’obésité infantile et adulte, le diabète de type 2, le cancer des testicules et la cryptorchidie, l’infertilité masculine, le TDAH et l’autisme.
Pour la majorité des situations examinées, les auteurs ont évalué la FA sur la base des éléments de preuve disponibles dans la littérature scientifique concernant la relation dose-réponse entre chaque PE et chaque maladie ou problème de santé investigués, ainsi que l’exposition de la population européenne, déterminée principalement à partir des données de biosurveillance disponibles. Le niveau de preuve a été déterminé par une approche de recherche de consensus d’experts (méthode itérative « Delphi »). Dans les cas, rares selon les auteurs, où des relations doses-réponses épidémiologiques n’étaient pas disponibles, le calcul de FA a été effectué en s’appuyant sur le risque relatif (RR) d’une maladie pour une exposition au PE considéré :
Équation 2
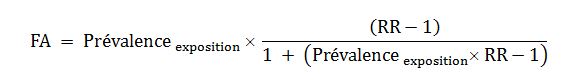
Finalement, l’incertitude inhérente à l’attribution d’un lien de causalité entre l’exposition à un PE et un problème de santé a été prise en considération. Pour ce faire, une « probabilité de causalité », variant de très faible (< 20 %) à très élevée (> 90 %), a été déterminée par le comité d’experts pour chaque combinaison PE-maladie examinée, à l’aide d’une matrice d’indices de robustesse des données tirées des études épidémiologiques et toxicologiques disponibles. Ces indices ont eux-mêmes été déterminés à partir de grilles d’analyses standardisées. Enfin, le résultat de l’équation 2 ci-dessus a été multiplié, à chaque itération de Monte-Carlo, par une variable dichotomique dont la fréquence de valeur prise (1 ou 0) dépend de la probabilité définie ci-dessus. Par exemple, pour un problème de santé déterminé à 80 % de certitude par le panel d’experts comme étant consécutif à l’exposition à un PE donné, la variable dichotomique décrite a pris la valeur de 1 dans 80 % des itérations de Monte-Carlo, et de 0 dans les 20 % restantes.
Résultats de l’étude
Le comité d’experts a jugé que la probabilité de causalité était forte (>70 %) entre la perte de QI et l’exposition aux PBDE et aux OP. Elle était jugée de moyenne à modérée (20-69 %) entre l’obésité et le diabète à la suite d’une exposition à divers phtalates, au DDE et au BPA, ainsi qu’entre les affections testiculaires et l’infertilité masculine et respectivement les PBDE et certains phtalates. Finalement, la probabilité de causalité entre les expositions dites « multiples » (non définies) ainsi que le TDAH et l’autisme a été jugée respectivement comme modérée (20-69 %) et faible (20-39 %).
Il y aurait 50 % de probabilité que les coûts estimés pour tous les PE et problèmes de santé qui découlent de leur exposition soient de 157 milliards d’euros annuellement, soit 1,23 % du PIB. En considérant l’incertitude sur les coûts, un intervalle d’estimation variant entre 117 et 175 milliards d’euros a été obtenu. De manière plus minimale, il y aurait 90 % de chance que les coûts associés aux effets directs et indirects découlant de l’exposition aux PE en Europe soient d’au moins 15,8 milliards d’euros.
Conclusion
Les auteurs attirent l’attention sur l’aspect inédit de leurs travaux et, effectivement, l’exercice de probabilité de causalité est particulièrement original puisqu’il est généralement réservé à la classification des substances cancérigènes. Ils concluent qu’il y a une probabilité substantielle que les coûts directs et indirects découlant de l’exposition aux PE en Europe soient très élevés et recommandent que cela soit considéré dans le processus de réglementation visant la gestion des risques et des prises de décision associés aux PE.
Les auteurs demeurent toutefois silencieux sur le fait qu’ils n’ont pas considéré les bénéfices sanitaires indirects de ces produits (par exemple, la diminution du nombre de cas de grands brûlés à traiter résultant de la présence de retardateurs de flamme dans les objets ménagers). De plus, ceux-ci font peu de cas de la nature très subjective du jugement d’experts, qui constitue pourtant la pierre d’assise de leur méthodologie, et ils ne détaillent pas la façon dont l’exposition moyenne de la population a été estimée à partir des données de biosurveillance ou autres. Ainsi, il s’avère impossible de reproduire leur analyse avec les éléments fournis dans l’article.
À la lumière de ces limites, et considérant la controverse entourant l’effet réel des PE sur l’humain (Middlebeek et Veuger, 2015; Dietrich et al., 2013; Nohynek et al., 2013), on peut considérer délicat le fait d’appuyer sur cette étude la mise sur pied d’une réglementation ayant un impact potentiel aussi important sur la société, même si d’un point de vue académique, l’approche utilisée demeure intéressante. En effet, il est clair que la question des PE revêt une importance considérable dans le domaine de la santé publique. Ceci dit, d’aucuns pourraient raisonnablement suggérer que l’exercice de Trasande et al. (2015) soit reproduit et fasse l’objet d’analyses approfondies avant de servir de base à un projet réglementaire. D’ailleurs, les auteurs admettent que « plus de recherche permettrait une estimation plus précise, mais prendrait beaucoup de temps et de ressources ».
Références
- Dietrich D., von Aulock S., Marquardt H. W., Blaauboer B. J., Dekant W., Kehrer J., Hengstler J. G., Collier A. C., Gori G. B., Pelkonen O., Lang F., Nijkamp F. P., Stemmer K., Li A., Savolainen K., Hayes A. W., Gooderham N., Harvey A. « Open letter to the European Commission: scientifically unfounded precaution drives European Commission's recommendations on EDC regulation, while defying common sense, well-established science, and risk assessment principles ». Arch Toxicol. 2013 Sept.;87(9):1739-41.
- Middelbeek R. J., Veuger S. A. « Letter to the Editor: Re: Neurobehavioral Deficits, Diseases, and Associated Costs of Exposure to Endocrine-Disrupting Chemicals in the European Union ». J Clin Endocrinol Metab. 2015 June;100(6):L52-3.
- Nohynek G. J., Borgert C. J., Dietrich D., Rozman K. K. « Endocrine disruption : fact or urban legend? ». Toxicol Lett. 2013 Dec. 16;223(3):295-305.
- Trasande L., Zoeller R. T., Hass U., Kortenkamp A., Grandjean P., Myers J. P., DiGangi J., Bellanger M., Hauser R., Legler J., Skakkebaek N. E., Heindel J. J. « Estimating burden and disease costs of exposure to endocrine-disrupting chemicals in the European union ». J Clin Endocrinol Metab. 2015 Apr.;100(4):1245-55.

