Plomb
Cette fiche technique est destinée aux autorités de santé publique dans l’exercice de leur mission.
Si la présence de plomb dans l’eau que vous consommez vous préoccupe, vous pouvez consulter la page du gouvernement du Québec et la page du gouvernement du Canada. Si vous désirez en savoir davantage sur les moyens de réduire votre exposition au plomb, vous pouvez également consulter cette autre page du gouvernement du Québec.
Sur cette page
Le plomb dans l’environnement
Le plomb (CAS RN 7439-92-1) est un métal grisâtre et inodore que l’on retrouve dans la croûte terrestre. Le plomb existe sous forme métallique, inorganique et organique.
Le plomb métallique est très peu soluble dans l’eau, très malléable et résistant à la corrosion, d’où sa large utilisation dans la fabrication de conduites d’eau dans le passé. Dans l’eau potable, le plomb existe majoritairement sous forme inorganique. Quant au plomb organique, il a été utilisé comme additif pour augmenter l’indice d’octane dans l’essence, jusqu’à ce qu’il soit interdit dans les années 19901.
Son omniprésence dans l’environnement (air, eau, sol, aliments) est presque exclusivement issue de l’activité humaine, comme1 :
- l’extraction et la fusion du minerai de plomb ou contenant du plomb;
- son utilisation passée dans l’essence des véhicules routiers, la peinture des vieilles maisons, dans les conduites d’eau et la robinetterie;
- son utilisation actuelle dans les carburants des petits aéronefs.
Le plomb dans l’eau potable
Le plomb est très peu présent dans les eaux naturelles. Sa présence dépend en partie du pH et de la teneur en sels dissous1.
Le plomb dans l’eau potable provient de la corrosion de composantes de la robinetterie ou de soudures contenant du plomb1, 2. Certains facteurs ont un impact sur le relargage du plomb dans l’eau potable, dont l’équilibre chimique de l’eau (p. ex. pH, alcalinité, température, etc.) et le temps de séjour de l’eau dans la tuyauterie1.
Lorsqu’elles sont présentes, les entrées de service en plomb contribuent largement aux concentrations mesurées dans l’eau potable d’un bâtiment1. La problématique de plomb dans l’eau potable au Québec touche un petit nombre de systèmes de distribution, mais quelques grandes villes en font partie. Les entrées de service contenant du plomb ont principalement été installées entre les années 1940 et 19552. Conséquemment, le remplacement complet de ces entrées de service constitue une des principales stratégies de réduction du plomb dans l’eau potable.
En savoir plus sur les concentrations de plomb mesurées dans l’eau potable au Québec
Afin de se conformer aux exigences du Règlement sur la qualité de l’eau potable (RQEP), les responsables de systèmes de distribution sont tenus de réaliser un certain nombre de prélèvements à l’eau distribuée pour vérifier le respect de la norme pour le plomb.
Entre 2013 et 2018, la concentration moyenne de plomb mesurée au Québec en vertu du RQEP (calculé sur plus de 44 000 échantillons) était de 4,0 µg/L et la concentration médiane, de 1 µg/L 3. La concentration maximale mesurée au cours de cette même période était de 977 µg/L pour l’année 2014, mais inférieure à 400 µg/L pour les autres années. Durant cette période, l’eau de 185 systèmes de distribution (sur un total de 2 931) a dépassé la norme alors en vigueur de 10 µg/L 3. Cette norme est passée à 5 µg/L en 20211.
Parallèlement aux mesures exigées dans le cadre du RQEP, un vaste programme de dépistage du plomb a été mené sur les fontaines et les robinets utilisés pour la consommation d’eau potable des écoles du Québec de 2019 à 20214. Les données sont présentées dans un rapport produit par le ministère de l’Éducation.
L’objectif poursuivi (p. ex. détection des sources de plomb, estimation de l’exposition au plomb ou évaluation de la conformité) et la méthode de prélèvement y étant associée sont à prendre en compte dans l’interprétation des concentrations de plomb retrouvées dans l’eau potable1.
Exposition de la population
Données de biosurveillance
Les données de biosurveillance dans la population permettent d’évaluer l’exposition des individus à l’ensemble des sources (aliments, eau, air, sol, produits de consommation). Elles ne permettent pas de distinguer l’apport spécifique de l’eau.
Le plomb peut être mesuré dans le sang, l’urine, les ongles, les cheveux, les os ou les dents1,5. La concentration du plomb dans le sang (plombémie) demeure le marqueur de choix pour la biosurveillance. Le plomb sanguin est un bon biomarqueur de l’exposition récente au plomb, puisque la demi-vie du plomb y est beaucoup plus courte que dans les os (environ 30 jours plutôt qu’une vingtaine d’années). Cependant, un seul prélèvement ne permet pas de distinguer une exposition chronique ou sous-chronique à de faibles niveaux de plomb d’une exposition aiguë à des niveaux élevés5.
En savoir plus sur les données de plombémie mesurées au Québec
Le seuil de déclaration obligatoire du plomb dans le sang par les laboratoires au Québec est de 5 µg/dL (0,25 µmol/L) pour les enfants âgés de 11 ans et moins et de 10 µg/dL (0,5 µmol/L) pour les individus âgés de 12 ans et plus6.
L’enquête canadienne sur les mesures de santé (ECMS) mesure chez des Canadiens et Canadiennes les concentrations de plomb dans le sang7.
Dans le cadre de l’ECMS, des données ont été recueillies auprès de personnes québécoises âgées de 3 à 79 ans. Le plomb est détecté dans plus de 99 % des échantillons analysés, ce qui témoigne de l’omniprésence du plomb dans l’environnement8.
Selon les résultats les plus récents (2016-2019), la moyenne géométrique du plomb, mesurée chez ces 2 192 personnes, est de 0,96 µg/dL de sang. Le 95e centile de la distribution est de 2,8 µg/dL de sang8.
Dans les années précédentes (2012-2015), la moyenne géométrique au Québec était de 1,2 µg/dL et le 95e centile était de 3,6 µg/dL8. Les données plus récentes indiquent donc une diminution de l’exposition globale des Québécois et Québécoises au plomb.
Toutefois, les concentrations sanguines de plomb chez la population québécoise tendent à être un peu plus élevées que celles obtenues dans le reste du Canada, mais cet écart est en diminution aussi.
Enfin, l’Institut national de santé publique du Québec (INSPQ) a modélisé l’effet des concentrations élevées, mais sporadiques de plomb dans l’eau potable sur la plombémie des enfants. Selon les scénarios simulés, il est possible, dans certaines situations plus problématiques, que ces expositions sporadiques résultent en une élévation significative de la plombémie chez les enfants exposés10.
Principales sources d’exposition
La population est principalement exposée au plomb par la nourriture et l’eau et, dans une moindre mesure, par l’air, le sol et les produits de consommation1.
Bien que les concentrations puissent être élevées dans les épices et certains gibiers chassés avec des munitions de plomb, les aliments qui contribuent le plus à l’apport en plomb sont les boissons (p. ex. café, thé, boissons gazeuses, vin ou bière), les légumes et les aliments à base de céréales1.
Les individus habitant un milieu résidentiel avec de vieilles peintures peuvent être exposés au plomb par l’intermédiaire des poussières intérieures 1,5.
Certaines sources ponctuelles comme les aéroports ayant un haut trafic de petits aéronefs ainsi que des installations industrielles sont susceptibles d’émettre plus de plomb dans l’air et, indirectement, de contaminer les sols 1,11. La population qui vit à proximité de ces sources est donc susceptible d’être davantage exposée au plomb par inhalation et par ingestion que la population générale.
En savoir plus sur les doses quotidiennes d’exposition au plomb par les aliments et par l’eau
Selon Santé Canada, chez la population générale canadienne de tous les âges, la dose quotidienne moyenne d’ingestion de plomb par les aliments est estimée à 0,1 µg/kg de p.c./jour, l’exposition étant généralement plus élevée chez les enfants et diminuant avec l’âge1. En effet, le taux d’ingestion des enfants par rapport à leur poids corporel est plus élevé que celui des individus plus âgés. Selon les données canadiennes de 2003 à 2007, l’exposition par ingestion chez les nourrissons se situerait en moyenne autour du triple de la valeur moyenne pour la population générale12, soit environ 0,3 µg/kg de p.c./jour.
La dose quotidienne de plomb associée à l’ingestion d’eau potable à 5 µg/L est de 0,085 µg/kg de p.c./jour (tableau 1). Cette dose est inférieure à la dose quotidienne moyenne alimentaire de 0,1 µg Pb/kg de p.c./jour pour la population générale. À partir de 6 µg/L la dose quotidienne de la population générale par l’eau potable rejoint la dose quotidienne moyenne alimentaire.
Chez les nourrissons, des concentrations plus basses dans l’eau potable, soit à partir de 4 µg/L, pourraient suffirent à engendrer une dose d’exposition quotidienne par l’eau potable (0,316 µg Pb/kg de p.c./jour) supérieure à la dose d’exposition quotidienne moyenne par les aliments (0,3 µg Pb/kg de p.c./jour au minimum).
Dose quotidienne moyenne d’exposition par l’eau potable | |||||
| Concentration de plomb dans l’eau potable (µg/L) | 1C | 4 | 5D | 6 | 10E |
| Population généraleA | 0,017 | 0,068 | 0,085 | 0,102 | 0,170 |
| NourrissonsB | 0,079 | 0,316 | 0,395 | 0,474 | 0,790 |
En gras : dose quotidienne moyenne d’exposition de plomb par l’eau potable supérieure à la dose d’exposition moyenne quotidienne de plomb par les aliments, soit 0,1 µg/kg de p.c./jour pour la population générale 1 ou environ 0,3 µg/kg de p.c./jour au minimum pour les nourrissons 12.
Notes de bas de tableau
A Dose quotidienne moyenne d’exposition par l’eau potable pour la population générale = (concentration de Pb dans l’eau) × (taux quotidien moyen d’ingestion d’eau de 0,017 L/kg de p.c./jour) chez les 0 à ≤ 80 ans 13.
B Dose quotidienne moyenne d’exposition par l’eau potable chez les nourrissons = (concentration de Pb dans l’eau) × (taux quotidien moyen d’ingestion d’eau de 0,079 L/kg de p.c./jour) chez les 0 à < 1 an 13.
C Concentration médiane de plomb dans l’eau potable mesurée au Québec entre 2013 et 2018 3.
D Norme pour le plomb selon le RQEP 14.
E Ancienne norme québécoise et canadienne pour le plomb dans l’eau potable.
Voies d’exposition par l’eau potable
L’ingestion est la principale voie d’absorption du plomb par l’eau potable, puisque la plupart des formes du plomb sont peu volatiles pour être inhalées. Le contact cutané par l’eau potable est une voie d’absorption négligeable (moins de 1 % de la dose appliquée)1.
Le plomb dans l’eau potable est inodore, sans saveur et ne colore pas l’eau.
Toxicocinétique
La toxicocinétique réfère aux processus d’absorption, de distribution, de métabolisation et d’excrétion des substances dans le corps après une exposition.
| AbsorptionA | Entre 40 % et 50 % de la dose ingérée chez les enfants et entre 3 % et 10 % chez les adultes |
|---|---|
| Distribution | Principalement dans les os, les tissus mous et le sang |
| Métabolites | Forme des complexes avec des macromolécules de l’organisme |
| Élimination | Environ 30 jours (sang); ≥ 20 ans (os) |
| Bioaccumulation | Os (jusqu’à 90 % du plomb ingéré) |
| Traverse la barrière placentaire? | Oui |
| Transféré au lait maternel? | Oui |
A Le jeûne, de même qu’une carence en fer et en calcium, peuvent accroître significativement l’absorption du plomb.
Effets à la santé
L’exposition chronique, sous-chronique et court terme au plomb peut entraîner plusieurs effets sur la santé chez l’humain1,5,11. L’exposition sous-chronique et chronique au plomb est associée à des effets sur tous les systèmes du corps pour des plombémies inférieures à 10 µg/dL5. Les effets à court terme sont plutôt associés à des plombémies 10 fois supérieures à celles pour les effets liés à des expositions sous-chroniques ou chroniques5. Le lien causal avec l’exposition est démontré pour certains des effets, alors que d’autres sont plutôt jugés probables ou possibles selon le niveau de preuves.
Les atteintes observées chez l’adulte découlent surtout de résultats d’études épidémiologiques menées auprès de populations humaines exposées au plomb, souvent en contexte professionnel. Les études épidémiologiques chez l’enfant reflètent plutôt une exposition provenant de l’environnement.
Même si le plomb cause de nombreux effets, ces derniers ne surviennent pas tous aux mêmes doses. Les effets du plomb sont généralement associés à des niveaux de plomb dans le sang (ou dans les os) plutôt qu’à des doses d’exposition. Pour connaître les plombémies auxquelles surviennent ces effets, voir la section Relations dose-réponse.
En savoir plus sur les effets sur la santé du plomb selon les organismes de référence
Une multitude d’études sont publiées depuis des décennies sur les effets sur la santé du plomb. L’évaluation du poids de la preuve, issue des résultats de ces études, a été effectuée par plusieurs organismes reconnus par le Groupe scientifique sur l’eau (GSE) de l’INSPQ 1,5,11,15–20 (voir aussi l’annexe Approche méthodologique).
La description des effets santé présentés ci-dessous s’appuie principalement sur les constats de l’U.S. Environmental Protection Agency (U.S. EPA) de 2024 11, à l’exception des effets cancérigènes qui reposent principalement sur l’évaluation du Centre international de Recherche sur le Cancer (CIRC) de 2006 16. L’évaluation de l’U.S. EPA réalisée en 2024 a été retenue pour soutenir la rédaction de la fiche, puisque le lien causal a été évalué plus spécifiquement et qu’il s’agit de la publication la plus récente 11. L’Agency for Toxic Substances and Disease Registry (ATSDR) 5 et Santé Canada 1 ont procédé à leur évaluation respectivement en 2020 et en 2019. Ces deux publications somme toute récentes ont été utilisées en complémentarité.
Exposition chronique
L’exposition chronique correspond à une exposition répétée à une substance pendant plusieurs années, généralement plus de 10 % d’une vie (p. ex. > 7 ans pour un humain dont la durée de la vie est fixée à 70 ans lors des évaluations du risque).
Effets cancérigènes
Les composés inorganiques du plomb sont considérés comme probablement cancérigènes pour l’humain (groupe 2A). La preuve est jugée suffisante pour la cancérogénicité des composés inorganiques du plomb chez les animaux de laboratoire par ingestion ou par injection sous-cutanée, mais elle est jugée insuffisante chez l’humain16.
L’interprétation des données dans les études épidémiologiques est souvent compromise par la présence d’autres substances concomitantes et l’omission du contrôle de certains facteurs de confusion. Les cancers relevés chez les animaux incluent les cancers du poumon, des glandes surrénales, des testicules, de la prostate, du cerveau et du rein, ce dernier étant le plus sensible et pour lequel les preuves sont les plus probantes 1,5,11,16,18.
Parmi les composés inorganiques étudiés, l’acétate de plomb, le sous-acétate de plomb, le phosphate de plomb et le chromate de plomb ont induit des cancers chez les animaux. L’arséniate de plomb et l’oxyde de plomb n’ont, quant à eux, pas mené au développement d’un cancer 1,16,18.
Effets non cancérigènes
L’exposition chronique au plomb dans l’eau potable cause plusieurs effets au niveau du système nerveux central, cardiovasculaire, hématologique, rénal, reproductif et neurodéveloppemental. Il est aussi probable qu’elle cause des effets sur le système immunitaire, des os et des effets psychopathologiques (p. ex. anxiété et dépression) 1,5,11.
Le lien entre l’exposition au plomb et les effets chez l’adulte est principalement appuyé par des données épidémiologiques chez des travailleuses et travailleurs exposés au plomb et, donc, davantage exposés que la population générale1,11.
En savoir plus sur les effets non cancérigènes du plomb
Le tableau 3 détaille les effets non cancérigènes qui découlent d’une exposition chronique au plomb selon l’évaluation de l’U.S. EPA de 202411. La section Relations dose-réponse présente les doses associées à ces effets.
| Organe ou système cible | Effet(s) |
|---|---|
| Système nerveux | Diminution de la fonction cognitiveA,B |
| Système cardiovasculaire | Augmentation de la tension artérielle/hypertensionB Maladies coronariennesB Mortalité associée à des problèmes cardiovasculairesB |
| Reins | NéphrotoxicitéB Diminution de la fonction rénaleB |
| Système reproducteur | Retard de maturation sexuelleA Altération de la production et de la qualité du sperme (concentration, motilité, viabilité, morphologie)B |
| Sang | Diminution de la survie et de la fonction des globules rougesA,B Altération de la synthèse de l’hèmeA,B AnémieA,B |
A Effet chez l’enfant.
B Effet chez l’adulte.
Au-delà des effets avérés, il existe d’autres effets rapportés en relation avec une exposition chronique au plomb pour lesquels le niveau de preuve permet de qualifier ce lien comme étant probable, possible ou encore insuffisant 11. Ces effets ainsi que le niveau de preuve sont présentés dans le tableau 4 ci-dessous.
| Lien entre l’exposition chronique au plomb et les effets observés | Effet(s) |
|---|---|
| Probable | Risque accru de psychopathologies (p. ex. comportements anxieux)B Atteinte de la fonction reproductrice de la femme (p. ex. ménopause précoce)B Effets sur les os et les dents (p. ex. diminution de la croissance osseuse ou de la formation de l’émail)A, B Susceptibilité accrue aux infections, changements dans les indicateurs d’immunité et de réponse inflammatoireA,B |
| Possible | Atteinte de l’audition ou de la vision (effet neurologique)A, B Autres effets cardiovasculaires (p. ex. athérosclérose)B Sensibilisation aux allergènes Effets hépatiques |
| Insuffisant | Autres effets neurologiques comme le tremblement essentiel ou l’accélération de la neurodégénérescence et de la démenceB Auto-immunité Effets gastro-intestinaux (coliques abdominales et de l’inconfort ou de la douleur, des nausées, des vomissements, une diarrhée ou de la constipation) Effets oculaires (non neurologiques) Effets endocriniens Effets respiratoires |
A Effet chez l’enfant.
B Effet chez l’adulte.
Exposition sous-chronique
L’exposition sous-chronique correspond à une exposition répétée à une substance allant de 30 jours à 10 % d’une vie (p. ex. < 7 ans par défaut pour un humain dont la durée de la vie est fixée à 70 ans lors des évaluations du risque).
L’effet du plomb sur le développement neurologique de l’enfant est aussi appuyé par un nombre considérable de données1,5,11. Les effets neurologiques et neurodéveloppementaux sont les plus documentés et de nombreuses études soutiennent un lien causal entre la plombémie et ces effets, principalement la diminution du quotient intellectuel (QI) chez les enfants 11. La section Relations dose-réponse présente les doses associées à ces effets. D’autres effets pouvant probablement résulter d’une exposition sous-chronique sont également présentés dans la section En savoir plus sur les effets d’une exposition sous-chronique au plomb ci-dessous.
En savoir plus sur les effets d’une exposition sous-chronique au plomb
| Lien entre l’exposition chronique au plomb et les effets observés | Effet(s) |
|---|---|
| Causal | Effets neurodéveloppementaux : Altération du comportementA (attention, impulsivité et hyperactivité) Diminution de la fonction cognitiveA |
| Probable | Risque accru de comportements d’internalisation (anxiété, dépression)A Risque accru de comportements d’externalisation (troubles du comportement, agressivité, comportement criminel)A Diminution de la fonction auditive et motriceA Risque d’avortements spontanés, de naissances prématurées, de faible taille et poids à la naissance (exposition durant la grossesse)B |
A Effet chez l’enfant
B Effet sur le fœtus
La diminution du QI chez les enfants est identifiée comme l’effet le plus sensible découlant d’une exposition au plomb. Bien que cet effet soit plus ou moins détectable sur le plan individuel, l’impact au niveau de la population peut être important1. À noter que durant la grossesse, un relargage du plomb accumulé dans les os de la mère au cours de sa vie contribue également à l’exposition totale de la mère et du fœtus.
Exposition à court terme
L’exposition à court terme correspond à une exposition répétée à une substance allant de plus de 24 heures à 30 jours.
L’exposition à court terme à des doses importantes de plomb occasionnerait principalement des effets neurologiques, gastro-intestinaux et musculosquelettiques (p. ex. apathie, irritabilité, faible capacité d’attention, céphalées, étourdissements, faiblesse, perte de mémoire, douleur épigastrique, constipation, vomissements, anorexie, paresthésie, anémie, convulsions, etc.). Une intoxication sévère peut mener à une encéphalopathie (convulsions, coma) et à la mort1,5,11. Les enfants sont plus vulnérables à une intoxication au plomb que les adultes, principalement parce que leur taux d’absorption est beaucoup plus élevé (voir tableau 2) et les effets sont plus durables (cerveau en développement).
Les effets aigus rapportés se basent sur de nombreuses études de cas, découlant principalement d’expositions en milieu de travail. Des relations dose-réponse pour ces effets ne peuvent être établies à partir de ces données, mais des plombémies sanguines au-delà desquelles ces effets pourraient survenir sont tout de même proposées (voir section Relations dose-réponse ci-dessous)5.
Relations dose-réponse
La plupart des effets neurologiques sont généralement rapportés pour des plombémies entre 1,3 et 10 µg/dL. L’effet le plus sensible d’une exposition au plomb est celui sur le développement neurologique des enfants (baisse du QI, à l’échelle de la population). Il n’existe aucune preuve d’un seuil pour cet effet. Bien que de manière globale, le QI diminue en fonction de la concentration de plomb dans le sang, il est observé que l’amplitude de l’impact de l’exposition au plomb sur la baisse du QI chez les enfants est plus importante pour de faibles plombémies sanguines que pour des plombémies élevées11. Cela veut dire que, bien que les conséquences augmentent avec la dose, cette augmentation est plus drastique à faible dose et plus subtile pour les doses élevées.
Les effets sur la maturation sexuelle peuvent se produire à des concentrations sanguines aussi basses que 1,3 µg/dL1. Les autres effets sur la reproduction sont associés à des plombémies se situant entre 3 et 24 µg/dL, et sont généralement plus cohérents entre les études à des plombémies supérieures à 10 µg/dL1,5.
Les effets cardiovasculaires, hématologiques et rénaux associés à une exposition chronique au plomb sont généralement relevés à des plombémies entre 2 et ˃ 20 µg/dL5.
Les symptômes cliniques d’une intoxication aiguë se manifestent généralement lorsque la plombémie dépasse les 30 µg/dL et leur sévérité augmente également avec les concentrations sanguines de plomb. L’encéphalopathie surviendrait à partir d’une plombémie de 100 µg/dL chez l’enfant et environ le double chez l’adulte5.
En savoir plus sur les relations dose-réponse du plomb
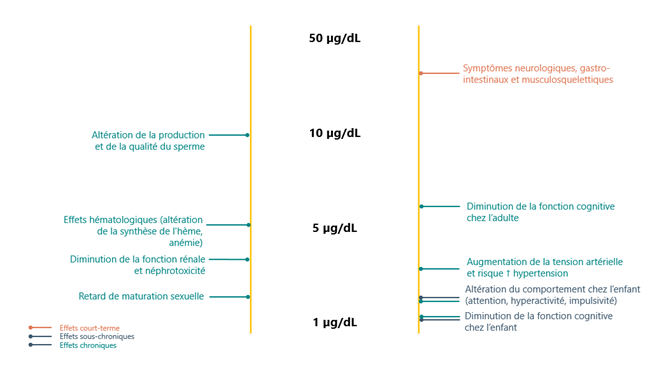
À cause de la longue demi-vie du plomb dans les os et de l’ensemble des facteurs qui peuvent l’affecter, il est difficile de tenir compte de la charge préexistante de plomb dans les études. Par conséquent, la plupart des études épidémiologiques tendent à établir un lien entre les effets et la plombémie plutôt qu’avec des doses externes d’exposition. Les principaux effets découlant d’une exposition au plomb sont présentés à la figure 1 en fonction de la plombémie la plus faible associée à chacun des effets dans les études épidémiologiques.
Plus la valeur de la plombémie associée à un effet néfaste est faible, plus cet effet est sensible.
Figure 1 – Concentrations minimales de plomb dans le sang associées à chacun des effets aigus, sous-chroniques et chroniques du plomb pour lesquels un lien causal est établi
Mécanisme d’action
Le mécanisme d’action comprend l’ensemble des mécanismes biochimiques, cellulaires et physiologiques nécessaires pour que la substance produise un effet.
Le plomb perturbe de nombreux processus biologiques1,5. Les mécanismes proposés sont multiples, mais les données sont insuffisantes pour identifier le mode d’action menant à la baisse de QI ou aux autres effets neurodéveloppementaux.
En savoir plus sur le mode d’action du plomb
Comme pour les effets sur le système nerveux central, les mécanismes proposés pour l’effet du plomb sur la pression artérielle sont eux aussi variés, sans qu’un mode d’action précis ne soit établi1.
Le plomb n’interagit directement avec l’ADN qu’à des concentrations très élevées, peu susceptibles de découler d’une exposition environnementale. À des doses plus faibles, les preuves disponibles chez l’animal et dans les études de laboratoire suggèrent une génotoxicité indirecte causée par un stress oxydatif1,5.
Facteurs modifiants
Plusieurs facteurs sont susceptibles de modifier la force de l’association entre l’exposition à une substance et le risque d’effets sanitaires 21,22. La force de l’association peut ainsi être amplifiée (effet synergique) ou, au contraire, être atténuée (effet protecteur).
Les facteurs modifiants peuvent être inhérents à des groupes d’individus (p. ex. âge, genre, formes différenciées d’un même gène – polymorphisme génétique –, habitudes de vie). Il peut aussi s’agir d’une autre substance qui, lorsqu’on y est exposé, interagit avec la substance d’intérêt.
Interactions possibles avec d’autres substances
Un effet synergique est suggéré pour les expositions professionnelles entre le plomb et l’arsenic ou le cadmium sur les effets neurologiques, entre le plomb et le cadmium pour les effets sur la reproduction, et avec le mercure inorganique pour les effets sur les reins (5,11). Ces interactions ne sont pas aussi évidentes lorsqu’il s’agit d’expositions environnementales23.
La présence de zinc est associée à une diminution de la toxicité du plomb sur plusieurs systèmes, dont des effets cardiovasculaires, développementaux, rénaux et reproductifs5.
Groupes sensibles de la population
Les principaux groupes sensibles, c’est-dire-ceux qui, pour une même dose d’exposition par unité de poids corporel, peuvent présenter une réponse toxique accrue au plomb à cause de prédispositions, sont 1 :
- les nourrissons et les enfants (notamment pour les effets neurodéveloppementaux);
- les personnes hypertendues ou diabétiques (pour les effets rénaux indésirables);
- les personnes afrodescendantes, les femmes enceintes et les femmes ménopausées (pour les effets cardiovasculaires indésirables).
Un niveau élevé de stress, des facteurs génétiques, de même que certains facteurs nutritionnels peuvent aussi avoir un impact sur la relation entre l’exposition au plomb et les effets engendrés11.
Normes et valeurs guides de gestion pour l’eau potable
Les normes et les valeurs guides de gestion (VGG) prennent en compte les limites de faisabilité technique (limite analytique ou de traitement). Les normes sont légalement contraignantes alors que les VGG ne le sont pas.
Les normes et les valeurs guides de gestion (VGG) pour le plomb (tableau 6) dans l’eau potable sont de 5 ou 10 µg/L, selon les organismes. À noter que la valeur présentée par l’Organisation mondiale de la Santé (OMS) est une valeur provisoire. Comme les entrées de service et la robinetterie constituent les principales sources de plomb dans l’eau potable, ces valeurs guides s’appliquent aux concentrations mesurées au point d’utilisation (robinet) et sont fondées en partie sur des contraintes de traitement et d’analyses, puisqu’aucun seuil n’a été identifié pour les effets sanitaires.
| Organisme | Gouvernement du Québec | Santé Canada | U.S. EPA | OMS |
|---|---|---|---|---|
| Année (référence) | 2021 24 | 2019 1 | 2024 25 | 2016 26 |
| Valeur (µg/L) | 5 | 5+ALARA | 10 | 10+ALARA |
| Type | Norme | VGG | Norme | VGG provisoireB |
| Nom | Norme de qualité de l’eau potable | Concentration maximale acceptable (CMA) | Treatment technique (TT); Action levelA | Provisional guideline value |
| Durée d’exposition applicable | Chronique | Chronique | Chronique | Chronique |
| Fondée sur des contraintes analytiques ou de traitement? | Oui | Oui | Oui | Oui |
ALARA : les concentrations dans l’eau potable devraient être maintenues aussi basses qu’il soit possible d’atteindre (acronyme anglais de As low as reasonably achievable).
A Le plomb est régulé par un traitement technique (TT) qui requiert un contrôle de la corrosivité de l’eau. Des démarches supplémentaires sont nécessaires si plus de 10 % des échantillons d’eau du robinet dépassent le seuil d’action (action level).
B En 2011, cette valeur guide fondée sur des considérations sanitaires a été remplacée par une valeur provisoire pour rendre compte de la faisabilité du traitement, étant admis qu’il est difficile d’atteindre moins de 10 μg/L avec un traitement central.
Normes québécoises
Le RQEP prévoit que « Quiconque met à la disposition d’un utilisateur de l’eau destinée à la consommation humaine doit s’assurer qu’elle satisfait aux normes de qualité de l’eau potable définies à l’annexe 1 (article 3) ». Toutefois, les exigences de contrôle varient en fonction du nombre de personnes desservies par le système de distribution (voir section En savoir plus sur les exigences du RQEP pour le plomb). La norme pour le plomb est de 5 µg/L30. Il s’agit de la même valeur que la concentration maximale acceptable (CMA) de Santé Canada (voir la section Valeurs guides de gestion de Santé Canada).
Depuis septembre 2024, un Règlement sur le contrôle du plomb dans l’eau des prestataires de service de garde éducatifs est entré en vigueur. La norme à respecter est la même que celle prévue au RQEP (5 µg/L)27. Par ailleurs, les balises de la procédure visant à mesurer les concentrations de plomb dans l’eau des écoles du Québec sont aussi basées sur la même valeur de 5 µg/L 28.
En savoir plus sur les exigences du RQEP pour le plomb
| Exigences de contrôle | Systèmes de distribution d’eau qui desservent au moins 21 personnes : exigence de contrôle dans l’eau distribuée une fois par année entre le 1er juillet et le 1er octobre afin de vérifier la conformité (article 14.1 du RQEP). |
|---|---|
| Systèmes de distribution qui desservent moins de 21 personnes (incluant les installations privées individuelles) : pas d’exigence de contrôle, mais exigence de vérifier la conformité sans délai s’il y a motif de soupçonner que l’eau distribuée est non conforme à la norme de 5 µg/L (article 42, RQEP). | |
| Prélèvements | Selon les exigences de prélèvement prévues (articles 14.1, 30 et annexe 4 du RQEP). |
| Analyses | Selon les exigences d’analyse prévues (article 31 du RQEP). Au Québec, plusieurs laboratoires sont accrédités par le ministère de l’Environnement, de la Lutte contre les changements climatiques, de la Faune et des Parcs (MELCCFP) pour l’analyse du plomb dans l’eau potable (29). Le plomb fait partie du domaine d’accréditation 11. |
| Taux de conformité | Selon le dernier bilan de mise en œuvre du RQEP, le taux de conformité des systèmes assujettis au contrôle annuel était de 98,3 % entre 2013 et 2018 3. |
| Gestion des dépassements | Les obligations réglementaires s’appliquent à tous les systèmes de distribution d’eau concernés, à l’exception de ceux qui alimentent seulement une résidence (articles 34. 36, 36,2 et 40 du RQEP). Le ou la responsable doit indiquer dans son bilan annuel de qualité de l’eau distribuée, pour chaque dépassement de norme observé, les mesures prises pour corriger la situation et pour protéger toute personne utilisatrice contre les risques encourus (article 53.3) Voir aussi la rubrique Soutien à la gestion des risques en complément aux exigences du RQEP. |
Le guide d’interprétation du RQEP offre des explications complémentaires sur les différents articles du règlement30. Il existe aussi un guide pour le suivi du plomb dans le cadre du RQEP, destiné aux responsables des systèmes de distribution 31. Ce guide inclut des repères pour l’échantillonnage, l’interprétation des résultats et la production d’un plan d’action à la suite d’un dépassement de la norme.
Valeur guide de gestion de Santé Canada
Santé Canada recommande une concentration maximale acceptable (CMA) de plomb dans l’eau potable de 5 µg/L1. Cette CMA s’appuie sur les effets neurodéveloppementaux observés chez les enfants (diminution du QI) de même qu’une évaluation des capacités analytiques et de traitement.
Santé Canada spécifie aussi que les concentrations dans l’eau potable devraient être maintenues aussi basses qu’il soit possible d’atteindre (principe ALARA).
Valeurs guides sanitaires pour l’eau potable
Une valeur guide sanitaire (VGS) est une concentration dans l’eau potable qui correspond à un objectif optimal de santé. Contrairement à une VGG, elle ne prend pas en compte les contraintes potentiellement liées à son application (limite analytique ou efficacité de traitement). Pour certaines substances, la norme est fixée à la même concentration que la VGS. Une VGS peut aussi être utilisée en complément d’une norme ou, en son absence, pour soutenir l’évaluation et la gestion des risques sur la santé.
Les VGS sont construites de manière à protéger contre l’ensemble des effets chez l’humain, y compris les effets les plus sensibles (soit ceux qui apparaissent aux doses les plus faibles). Aussi, elles tiennent compte de facteurs d’incertitude qui protègent toute la population, y compris les groupes sensibles.
Les VGS sont donc strictement basées sur un risque négligeable d’effets néfastes, soit un risque pour lequel l’apparition d’effets cancérigènes ou non cancérigènes est improbable chez la population exposée 32. Ainsi, une exposition supérieure à la VGS ne signifie pas que la population exposée développera des effets néfastes.
Le tableau 7 détaille les VGS publiées par les organismes reconnus. Puisqu’aucun seuil n’est identifié pour les effets neurodéveloppementaux chez les enfants, la plupart des organismes recommandent que les concentrations de plomb dans l’eau potable soient aussi basses qu’il soit raisonnablement possible d’atteindre (ALARA).
L’écart entre les VGS et la norme de 5 µg/L s’explique par des enjeux liés aux capacités d’analyser et de traiter le plomb dans l’eau destinée à la consommation humaine.
Ces VGS s’appuient principalement sur des effets découlant d’une exposition sous-chronique, mais s’appliquent aussi dans le cas d’expositions de plus longue durée. Aucune VGS courte terme n’a été repérée parmi les organismes consultés.
| Organisme | Santé Canada | U.S. EPA | OEHHA |
|---|---|---|---|
| Année (référence) | 2019 1 | 2018 33 | 2009 34 |
| Valeur (µg/L) | ALARA | Objectif de zéroA | 0,2B |
| Nom de la VGS | Concentration acceptable dans l’eau potable qui présenterait un niveau de risque « essentiellement négligeable » | Maximum contaminant level goal (MCLG) | Public Health Goal (PHG) |
| Groupe d’âge | Enfants | S. O. | Enfants |
| Effet(s) le(s) plus sensible(s) retenu(s) | Diminution du QI | Diminution du QI | Diminution du QI |
| Dose de référence (VTR) | 0,4 µg/kg p.c./jourC | S. O. | 2,86 µg/jourC |
A Selon la réglementation américaine, une substance normée se voit attribuer automatiquement un maximum contaminant level goal (MCLG) de zéro s’il n’y a pas de dose sous laquelle l’exposition à cette substance est considérée comme sécuritaire 25.
B Concentration jugée protectrice de la population.
C Dose associée à une diminution de 1 point de QI.
Kg de p.c. : kilogramme de poids corporel; S. O. : sans objet.
En savoir plus sur la détermination des VGS pour le plomb
Les VGS sont déterminées à partir d’une valeur toxicologique de référence (VTR), laquelle s’appuie sur des doses repères ou point de départ (POD)35. Un POD est une dose d’exposition, exprimée en µg/kg de p.c./jour, obtenue à partir d’une analyse de la courbe dose-réponse. Aucun facteur d’incertitude n’est appliqué aux POD afin de tenir compte, par exemple, de la variabilité interindividuelle. Une VTR reflète le potentiel toxique des substances à l’égard de la santé humaine. Elle est fondée soit sur un effet toxique avec seuil de dose, soit sur un effet toxique sans seuil de dose.
S’il s’agit d’effets avec seuil, la VTR correspond à la dose de référence (RfD) exprimée en µg/kg de p.c./jour. En revanche, s’il s’agit d’effets sans seuil, la VTR correspond au risque unitaire (RU) exprimé en (µg/kg de p.c./jour)-1. Cette unité correspond, pour un effet désigné, à la proportion de cas supplémentaires estimés au sein d’une population exposée à 1 µg/kg de p.c./jour d’une substance donnée pendant la vie entière, par rapport à la proportion de cas attendus dans une population non exposée à cette même substance.
Pour dériver des VGS, le volume d’eau consommé quotidiennement est aussi utilisé35. De même, pour les effets non cancérigènes chroniques ou sous-chroniques, la contribution relative de l’exposition par l’eau potable sur l’exposition totale à la substance (RSC) est prise en compte. Pour les effets cancérigènes, un niveau de risque négligeable est aussi utilisé, habituellement de 1 × 10-6 ou 1 × 10-5.
Les VGS proposées peuvent varier pour un même effet critique en raison du type de POD ainsi que des paramètres choisis (p. ex. consommation d’eau et RSC). Le tableau 8 suivant détaille et compare les principaux paramètres utilisés pour la dérivation des VGS présentées au tableau 7.
| Organisme | Santé Canada | U.S. EPA | OEHHA |
|---|---|---|---|
| Année (référence) | 2019 1 | 2018 33 | 2009 34 |
| Valeur (µg/L) | ALARA | Objectif de zéroA | 0,2B |
| Nom de la VGS | Concentration acceptable dans l’eau potable qui présenterait un niveau de risque « essentiellement négligeable » | Maximum contaminant level goal (MCLG) | Public Health Goal (PHG) |
| Groupe d’âge | Enfants | S. O. | Enfants |
| Effet le plus sensible retenu | Diminution du QI | Diminution du QI | Diminution du QI |
| Dose de référence (VTR) | 0,4 µg/kg de p.c./jourC | S. O. | 2,86 µg/jourD |
Dose repère ou point de départ (facteur d’incertitude) | Plombémie de 1,2 µg/dL | S. O. | Plombémie de 1,0 µg/dL1 |
| Type de point de départ (POD) | BMDI01 | S. O. | BMDI01 |
| Espèce (étude clé) | Humain 36 | S. O. | Humain36 |
Consommation d’eau (litre/kg de p.c./jour) | 0,9L/jour | S. O. | 1 L/jour |
| Contribution relative de la source | S. O. | S. O. | 20 % |
A Selon la réglementation américaine, une substance normée se voit attribuer automatiquement un maximum contaminant level goal (MCLG) de zéro s’il n’y a pas de dose sous laquelle l’exposition à cette substance est considérée comme sécuritaire 25.
B Concentration jugée protectrice de la population; calculée en multipliant la VTR par la contribution relative de la source et en divisant par le produit de la consommation d’eau et du facteur d’incertitude de 3. Un facteur de 3 a été sélectionné à cause de l’absence de seuil pour l’effet critique.
C La VTR correspond à la dose associée à une diminution de 1 point de QI. En absence de seuil pour l’effet, Santé Canada a dérivé un coefficient de pente de 2 500 (mg/kg p.c./jour)-1; voir section En savoir plus sur la VGS de Santé Canada.
D Correspond au faible niveau préoccupant pour les enfants (12-24 mois) selon l’OEHHA. Dérivé à partir l’élévation de la plombémie associée à une diminution de 1 point de QI.
Kg de p.c. : kilogramme de poids corporel; S. O. : sans objet; H : humain.
Pour en savoir plus sur la manière dont sont dérivées les diverses VGS, consultez la Méthodologie d’élaboration de valeurs guides sanitaires chroniques pour les contaminants chimiques de l’eau potable 35.
Valeur guide sanitaire (VGS) de Santé Canada
Sur la base des études disponibles pour évaluer le lien entre la plombémie chez les enfants et la diminution du QI, il n’est pas possible d’identifier un seuil en dessous duquel il est possible d’assumer une absence d’effets. Santé Canada recommande donc que le plomb soit considéré comme une substance sans seuil. Par conséquent, plutôt que d’établir une VGS, il est demandé que tout soit mis en œuvre pour maintenir les concentrations de plomb dans l’eau potable au niveau le plus faible qu’il soit raisonnablement possible d’atteindre (ALARA).
En savoir plus sur la VGS de Santé Canada
Une valeur de risque unitaire (VTR) pour les effets cognitifs a été dérivée par Santé Canada. Cette valeur repose sur un POD qui correspond à la concentration de plomb dans le sang de 1,2 µg/dL associée à une diminution de 1 point de QI (BMDI01) déterminée par l’European Food Safety Authority (EFSA)37. Par la suite, la modélisation a permis de déterminer que la dose orale externe correspondante chez un enfant âgé de 5 ans serait de 0,4 µg/kg de p.c./jour. En divisant la réponse de référence (baisse de 1 point de QI) par la dose de 0,4 µg/kg de p.c./jour, un coefficient de pente de 2 500 (mg/kg p.c./jour)-1 a été obtenu1. À défaut de pouvoir établir un seuil d’exposition sans effet, cette démarche permet d’évaluer l’impact de la concentration dans l’eau potable sur le risque populationnel d’une diminution du QI.
Soutien à la gestion des risques
La gestion des risques liés à la présence de substances dans l’eau potable se fait au cas par cas, car elle tient compte de plusieurs facteurs comme l’ampleur du risque, la spécificité de la contamination, le contexte régional, l’applicabilité des options de gestion ou l’acceptabilité sociale. Des outils peuvent être utilisés afin de guider les autorités de santé publique à cet effet38–41.
Il est possible de consulter la page du gouvernement du Québec pour accéder à l’information divisée en sections spécifiques selon les principaux acteurs touchés par la présence de plomb dans l’eau potable 42.
Pour en savoir plus sur les mesures de traitement communautaires ou domestiques (ou individuel) du plomb dans l’eau potable, il est possible de se référer à Santé Canada1.
Dans le cas des purificateurs d’eau domestiques, il est important que ces derniers soient certifiés selon la norme NSF/ANSI31 et de les entretenir selon les indications du fabricant. D’autres pages Web peuvent être utiles à consulter pour ces méthodes de traitement43,44.
Références
- [En ligne]. Santé Canada. Recommandations pour la qualité de l’eau potable au Canada : document technique – le plomb; 2019 [cité le 3 févr 2025]. Disponible
- MELCC. Guide d’évaluation et d’intervention en lien avec le suivi du plomb et du cuivre dans l’eau potable [En ligne]. Ministère de l’Environnement et de la Lutte contre les changements climatiques; 2021 [cité le 5 févr 2025]. Disponible.
- MELCC. Bilan de mise en oeuvre du Règlement sur la qualité de l’eau potable 2013-2018 [En ligne]. Ministère de l’Environnement et de la Lutte contre les changements climatiques; 2020 [cité le 5 févr 2025]. Disponible.
- Ministère de l’Éducation. Bilan de l’opération de dépistage du plomb dans l’eau des écoles [En ligne]. Gouvernement du Québec; 2023. Disponible.
- Agency for Toxic Substances and Disease Registry (ATSDR). Toxicological profile for lead [En ligne]. Atlanta, GA: U.S. : Department of Health and Human Services, Public Health Service.; 2020. Disponible.
- Ministère de la Santé et des Services sociaux [En ligne]. MSSS. Seuils de déclaration par les laboratoires – Substances chimiques; 2019 [cité le 7 févr 2025]. Disponible.
- Gouvernement du Canada [En ligne]. Santé Canada. Sixième rapport sur la biosurveillance humaine des substances chimiques de l’environnement au Canada; 14 déc 2021 [cité le 7 févr 2025]. Disponible.
- Institut national de santé publique du Québec [En ligne]. INSPQ. Mise à jour du portrait d’imprégnation de la population québécoise aux substances chimiques de l’environnement issu de l’Enquête canadienne sur les mesures de la santé; 4 juill 2024 [cité le 7 févr 2025]. Disponible.
- Institut national de santé publique du Québec [En ligne]. INSPQ. Extraction des données québécoises de biosurveillance des substances chimiques de l’environnement issues de l’Enquête canadienne sur les mesures de la santé | INSPQ; 2 mai 2018 [cité le 7 févr 2025]. Disponible.
- Institut national de santé publique du Québec [En ligne]. Équipe scientifique sur l’eau, Équipe scientifique sur les risques toxicologiques et radiologiques. Présence de plomb dans l’eau des écoles et des garderies : importance du risque et pertinence d’une surveillance à chaque point d’utilisation | INSPQ; 13 juin 2019 [cité le 14 avr 2025]. Disponible.
- US Environmental Protection Agency [En ligne]. EPA CFPH& EA. Integrated Science Assessment (ISA) for Lead (Final Report); 2024 [cité le 18 mars 2025]. Disponible.
- [En ligne]. Santé Canada. Apports alimentaires en contaminants et en autres produits chimiques chez les Canadiens, selon les groupes d’âge et de sexe: 2001 (archivée); 30 janv 2009 [cité le 20 mars 2025]. Disponible.
- [En ligne]. Food Risk. What We Eat In America - Food Commodity Intake Database; s.d. [cité le 7 févr 2025]. Disponible.
- RQEP. Règlement sur la qualité de l’eau potable [En ligne]. Disponible.
- Anses. Expositions au plomb : effets sur la santé associés à des plombémies inférieures à 100 μg/L - Avis de l’Anses, rapport d’expertise collective. [En ligne]. Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail; 2013. Disponible.
- IARC Publications Website [En ligne]. IARC. Inorganic and Organic Lead Compounds; 2006 [cité le 5 févr 2025]. Disponible.
- NTP. NTP monograph, Health Effects of Low-level Lead [En ligne]. National Toxicology Program, U.S. Department of Health and Human Services; 2012 [cité le 5 févr 2025]. Disponible.
- National Toxicology Program (NTP). Report on Carcinogens, Fifteenth Edition [En ligne]. Department of Health and Human Services; 2021. Disponible.
- OEHHA. Public health goals for chemicals in drinking water - lead [En ligne]. Pesticide and Environmental Toxicology Branch, Office of Environmental Health Hazard Assessment, California Environmental Protection Agency; 2009. Disponible.
- [En ligne]. Santé Canada. Rapport final sur l’état des connaissances scientifiques concernant les effets du plomb sur la santé humaine; 2013 [cité le 5 févr 2025]. Disponible.
- Soto JC, Barakat M, Hutter JA, Warembourg C. Chapitre 12. Épidémiologie. Dans: Environnement et santé publique [En ligne]. Presses de l’EHESP; 2023 [cité le 7 mars 2025]. p. 305‑34. Disponible.
- Delva F, Lacourt A. Effet conjoint et interaction. Environnement, Risques & Santé. JLE Editions; 2020;191:67‑67.
- Valcke M, Ponce G, Bourgault MH, Perron S. Soutien scientifique aux autorités de santé publique dans le cadre du processus de renouvellement de l’autorisation ministérielle accordée à Glencore pour l’exploitation de la Fonderie Horne à Rouyn-Noranda [En ligne]. Institut National de Santé Publique du Québec; oct 2022. (Rapport d’évaluation du risque). Disponible.
- Gouvernement du Québec. RLRQ c Q-2, r 40 | Règlement sur la qualité de l’eau potable [En ligne]. CanLII; 2021 [cité le 20 mars 2025]. Disponible.
- US Environmental Protection Agency [En ligne]. EPA. National Primary Drinking Water Regulations; 2024 [cité le 21 mars 2025]. Disponible.
- OMS. Lead in Drinking-water, Background document for development of WHO Guidelines for Drinking-water Quality [En ligne]. Organisation mondiale de la santé; 2016. Disponible.
- Ministère de la Famille. Règlement sur le contrôle du plomb dans l’eau chez les prestataires de services de garde éducatifs. Gazette officelle du Québec . 156e année, no 35. Éditeur officiel du Québec; 28 août 2024;5531‑6.
- Gouvernement du Québec [En ligne]. Gouvernement du Québec. Plomb dans l’eau des écoles; 2025 [cité le 5 févr 2025]. Disponible.
- [En ligne]. Centre d’expertise en analyse environnementale du Québec (CEAEQ). Laboratoires accrédités offrant des services spécifiques à l’analyse de l’eau potable en conformité avec la réglementation en vigueur; [cité le 24 févr 2025]. Disponible.
- [En ligne]. Gouvernement du Québec. Guide d’interprétation du Règlement sur la qualité de l’eau potable; 2024.
- Gouvernement du Québec [En ligne]. MELCCFP. Guide d’évaluation et d’intervention en lien avec le suivi du plomb et du cuivre dans l’eau potable; [cité le 25 mars 2025]. Disponible.
- Bourgault M, Ponce G, Valcke M. Soutien à l’analyse des risques à la santé associés à la présence de PFAS dans l’eau potable de La Baie [En ligne]. Institut National de Santé Publique du Québec; 2023 [cité le 7 mars 2025]. Disponible.
- US EPA. 2018 Edition of the Drinking Water Standards and Health Advisories Tables [En ligne]. Office of Water U.S. Environmental Protection Agency Washington, DC; 2018 [cité le 5 févr 2025]. Disponible.
- Union Européenne. Directive (UE) 2020/2184 du Parlement européen et du Conseil du 16 décembre 2020 relative à la qualité des eaux destinées à la consommation humaine (refonte). [En ligne]. OJ L 16 déc 2020 p. 1‑62. Disponible.
- Institut national de santé publique du Québec [En ligne]. Bourgault M, Valcke M. Méthodologie d’élaboration de valeurs guides sanitaires chroniques pour les contaminants chimiques de l’eau potable; 2022 [cité le 24 févr 2025]. Disponible.
- Lanphear BP, Hornung R, Khoury J, Yolton K, Baghurst P, Bellinger DC, et al. Low-Level Environmental Lead Exposure and Children’s Intellectual Function: An International Pooled Analysis. Environ Health Perspect. juill 2005;113(7):894‑9.
- EFSA. Scientific Opinion on Lead in Food: Lead in Food. European Food Safety Authority (EFSA) Panel on Contaminants in the Food Chain (CONTAM). EFSA Journal. avr 2010;84:1570.
- Cortin V, Laplante L, Dionne M. La communication des risques à la santé [En ligne]. Institut National de Santé Publique du Québec; 2018 [cité le 7 mars 2025]. Disponible.
- Laplante L, Goulet J, Bolduc L. Gestion des risques liés aux urgences et aux sinistres chimiques au Québec : outil de prise en charge de la période critique [En ligne]. Institut National de Santé Publique du Québec; 2024 [cité le 7 mars 2025]. Disponible.
- Groupe de travail ad hoc sur l’élaboration du guide d’intervention lors de dépassement de normes chimiques dans l’eau potable. Outil d’aide à la décision lors de dépassement de normes ou de contaminations chimiques dans l’eau potable [En ligne]. Institut National de Santé Publique du Québec; 2015. Disponible.
- Institut national de santé publique du Québec. La gestion des risques en santé publique au Québec : cadre de référence [En ligne]. Institut National de Santé Publique du Québec; 2016 [cité le 7 mars 2025]. Disponible.
- Gouvernement du Québec [En ligne]. MELCCFP. Le plomb dans l’eau potable; [cité le 11 avr 2025]. Disponible.
- Mon eau - Mon puits - Ma santé [En ligne]. Mon eau - Mon puits - Ma santé. Que faire si votre eau contient des contaminants; [cité le 7 mars 2025]. Disponible.
- Gourvernement du Canada [En ligne]. Santé Canada. Eau potable et santé : Traitement; 3 juin 2024 [cité le 7 mars 2025]. Disponible.
- Bourgault MH, Ponce G, Valcke M. Méthodologie de recherche et de sélection de valeurs toxicologiques de référence publiées par les organismes reconnus [En ligne]. Canada : Équipe scientifique d’évaluation des risques toxicologiques et radiologiques, Institut national de santé publique du Québec; 2024. Disponible.
- Gouvernement du Québec. Règlement sur la qualité de l’eau potable [En ligne]. L.R.Q. Sect. chapitre Q-2, r. 40 2024. Disponible.
Annexe – Approche méthodologique
Le contenu des fiches synthèses repose principalement sur les revues toxicologiques effectuées par les organismes de référence cités dans la Méthodologie de recherche et de sélection de valeurs toxicologiques de référence (45). Cette recension permet de faire la revue des organismes qui ont évalué la substance de manière exhaustive, avec pour la plupart, une révision par les pairs. Elle constitue donc une base de données probantes des sources d’exposition, des mécanismes d’action et des principaux effets sur la santé retenus par ces organismes. Dans le cas du plomb, plusieurs sources ont été repérées 1,5,11,15–20.
D’autres sources peuvent également être consultées lorsque des données sont disponibles au sujet de la substance qui fait l’objet de la fiche synthèse. Elles complètent les informations extraites des sources citées ci-dessus : généralités sur les substances (p. ex. caractéristiques physico-chimiques, présence dans l’environnement), sources d’exposition, données de biosurveillance, toxicocinétique et effets sur la santé. Le GSE examine d’abord si de telles publications ont déjà été colligées en raison de travaux antérieurs sur la substance. Une recherche de la littérature grise peut aussi être effectuée. Les documents avec révision par les pairs et pour lesquels la méthodologie d’élaboration est explicite sont priorisés. De fait, des sources additionnelles avaient été repérées au début de la mise à jour de la fiche synthèse sur le plomb (3,4,6–8,12). Aussi, les effets sur la santé décrits dans la présente fiche synthèse s’appuient en grande partie sur les plus récentes évaluations, soit celles de l’U.S. EPA 11, de l’ATDSR 5 et de Santé Canada 1.
Les normes québécoises dans l’eau (Règlement sur la qualité de l’eau potable et autres si applicables) sont recensées (46). Les valeurs guides, soit les valeurs guides sanitaires (VGS) ou les valeurs guides de gestion (VGG) publiées par des organismes reconnus, sont également recensées pour des durées d’exposition à court terme, sous-chronique et chronique. Ces sources sont énumérées dans la Méthodologie d’élaboration de valeurs guides sanitaires chroniques pour les substances chimiques de l’eau potable 35. Une liste des sources de valeurs guides pour le plomb a pu être consolidée (1,19,25,26).
Enfin, le contenu des fiches synthèses est révisé auprès de collaboratrices et collaborateurs reconnus pour leur expertise dans le domaine et qui n’ont pas participé à la rédaction de la fiche. Ces collaborateurs et collaboratrices incluent des réviseurs et réviseuses internes à l’INSPQ (p. ex. membres du GSE ou de l’Équipe scientifique sur les risques toxicologiques et radiologiques [ESRTR]) ainsi que des réviseuses et réviseurs externes de l’INSPQ tels que des directions régionales de santé publique, des partenaires universitaires, des organisations de santé (p. ex. Santé Canada) ainsi que des ministères (p. ex. ministère de la Santé et des Services sociaux, ministère de l’Environnement, de la Lutte contre les changements climatiques, de la Faune et des Parcs).
Rédaction
Rédactrice : Axelle Marchand, conseillère scientifique, Institut national de santé publique du Québec
Sous la coordination de : Marie-Eve Levasseur, Institut national de santé publique du Québec
Collaboratrices : Vicky Huppé et Marie-Hélène Bourgault, Institut national de santé publique du Québec
Révision scientifique : Marc Yélian Bossou, centre intégré universitaire de santé et de services sociaux de la Côte-Nord
Gwendaline Kervran, centre intégré universitaire de santé et de services sociaux de la Capitale-Nationale
Mathieu Valcke, Caroline Huot, Michelle Gagné, Institut national de santé publique du Québec
Les réviseuses et les réviseurs ont été conviés à apporter des commentaires sur la version préfinale de ce document et en conséquence, n’en ont pas révisé ni endossé le contenu final.
Révision linguistique (texte seulement) : Aurélie Franco, Institut national de santé publique du Québec
Remerciements : le Groupe scientifique sur l’eau remercie Donald Ellis, Daria Pereg et Félix Légaré-Julien du ministère de l’Environnement, de la lutte contre les changements climatiques, de la Faune et des Parcs, pour leurs précisions concernant les exigences du Règlement québécois sur la qualité de l’eau potable pour le plomb.
Citation suggérée :
Groupe scientifique sur l’eau (2025). Plomb. Dans Fiches synthèses sur l’eau potable et la santé humaine. Institut national de santé publique du Québec. Disponible :
La présente fiche synthèse a été réalisée dans le cadre de l’entente spécifique La protection de la santé publique financée par le ministère de la Santé et des Services Sociaux.

