Infections causées par le virus du Nil occidental – profil épidémiologique
Problématique
Le virus du Nil occidental (VNO) a été isolé pour la première fois en 1937 en Ouganda. Il s’agit d’un virus à ARN, du groupe des Flaviviridae, dont fait partie, entre autres, le virus de l’encéphalite de Saint-Louis1-3. Le VNO est reconnu comme étant le plus répandu de ce groupe et son activité est endémique sur plusieurs continents1,4,5. Il a été la cause d’éclosions dans plusieurs pays d’Afrique, d’Asie de l’Ouest, du Moyen-Orient et d’Europe. Il a été également associé à des épidémies en Roumanie (1996 à 1998) ainsi que plus récemment, en Russie (1999), aux États-Unis (1999-2000) et en Israël (2000).
Le vecteur
Le moustique est le vecteur du VNO le plus souvent identifié. à ce jour, le virus a été isolé chez 43 espèces de moustiques à travers le monde. Le genre Culex est le plus fréquemment infecté. La tique pourrait aussi transmettre le VNO, mais ce mode de transmission n’a pas encore été observé en Amérique du Nord1,4.
Les moustiques se reproduisent dans les milieux aquatiques ou sur des sols humides. Ils se nourrissent de sève et de nectar de végétaux. La femelle doit piquer un mammifère afin de prélever le sang nécessaire à la ponte des œufs. Dans les régions tempérées, la femelle a tendance à ne piquer qu’une seule fois alors que plus au sud, elle aura la possibilité de piquer à plusieurs reprises. Certaines espèces de moustiques ont une préférence pour les oiseaux (ornithophiles) tandis que d’autres, dont Culex spp, piquent autant les oiseaux que les mammifères. La durée de vie d’un moustique adulte peut varier d’une semaine à plus de trente jours6.
La persistance du virus a été démontrée chez des moustiques femelles prélevés durant l’hiver; de même, la transmission trans-ovarienne du virus pourrait contribuer à maintenir le virus actif chez le vecteur bien que cela demeure controversé7.
Le réservoir
Seuls certains hôtes peuvent jouer un rôle de réservoir naturel du VNO. La présence du virus dans le sang circulant (virémie) doit être soutenue et suffisante pour entraîner une infection chez le moustique vecteur. Les oiseaux constituent le principal réservoir animal8. Par conséquent, pour transmettre le VNO aux humains et aux autres mammifères, les moustiques doivent avoir préalablement piqué un oiseau infecté. Au moins 76 espèces d’oiseaux peuvent être atteintes9. En Amérique du Nord, la famille des Corvidés est particulièrement sensible à l'infection qui est létale chez un fort pourcentage d'individus. Les espèces migratrices peuvent contribuer à amplifier l’importance du réservoir lors de leurs rassemblements dans les zones tropicales et subtropicales. Le VNO provoque chez l’oiseau une infection d’une durée limitée, qui se solde par la mort de l’animal, ou encore par la disparition de l’infection. La durée de la virémie est peu connue et varie selon les espèces10,11.
Les humains et plusieurs animaux, notamment les chevaux, sont des hôtes accidentels4,8. Les chevaux semblent sensibles aux effets de la maladie. En effet, lors de l’éclosion de New York en 1999, l’infection au VNO a été documentée chez 25 chevaux et 9 en sont morts12.
La transmission
Le VNO est classé dans le groupe des arbovirus, terme tirant son origine de « arthropod borne virus » (ou virus portés par les arthropodes), qui regroupe les virus se transmettant par piqûres d’insectes. À ce jour, il n’existe aucune preuve indiquant que le virus se transmet de l’animal à l’humain ou d’un humain à l’autre8.
La présentation clinique
L’infection due au virus du Nil occidental est une maladie saisonnière. Dans les régions tempérées, le risque d’une éclosion est plus élevé à la fin de l’été ou à l’automne13.
Le patient présente une fièvre d’une durée de 3 à 5 jours pouvant être accompagnée des symptômes suivants: céphalées sévères, adénopathies, éruptions cutanées généralement au tronc, symptômes gastro-intestinaux, douleurs oculaires et myalgies. Plus rarement, et particulièrement chez les personnes âgées, l’infection peut être plus sérieuse et causer une encéphalite ou une méningite. La faiblesse musculaire peut également être présente. Le traitement en est un de support, selon l’état du patient. Il n’existe pas de traitement spécifique ni de vaccin. L’infection semble conférer une immunité à vie4,8,14.
Il est estimé qu’environ 1 % des gens infectés développent une maladie cliniquement apparente15,16. De ce pourcentage, un nombre encore plus restreint développe une maladie grave. Les personnes âgées constituent un groupe plus vulnérable4. D’ailleurs, 60 % des gens cliniquement atteints lors de l’éclosion survenue à New-York en 1999 étaient âgés de 65 ans ou plus17.
Le diagnostic humain est généralement obtenu par sérologie. Le prélèvement de deux sérums (précoce et tardif) se fait avec un intervalle de 14 à 21 jours. Le diagnostic peut également être effectué à l’aide du liquide céphalo-rachidien (LCR). La confirmation de l’infection au VNO est basée sur les critères suivants : isolation du virus ou présence d’antigènes ou de séquences génomiques virales dans les tissus, le LCR ou le sang, et démonstration de la présence d’anticorps, notamment parla méthode ÉLISA3,4,14.
Les épidémies dues au VNO
Bien qu’elle soit devenue une préoccupation de santé publique largement médiatisée aux États-Unis, la maladie secondaire au VNO demeure très rare chez les humains tant en Europe qu’en Amérique du Nord. La présence de ce virus n’a pas encore été démontrée au Québec. Les récentes éclosions en Roumanie, en Russie et aux États-Unis démontrent que des épidémies sont possibles en climat tempéré14,18,19. Le tableau 1 présente quelques données d’épidémies d’infections dues au VNO survenues dans le monde.
Tableau 1. Synthèse de quelques épidémies d’infection au VNO survenues dans le monde entre 1950 et 2000
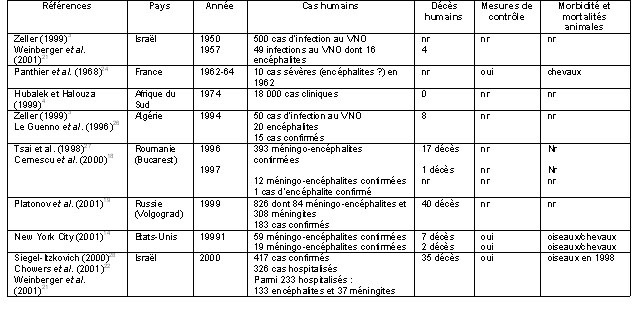
nr: non rapporté
Il est intéressant de noter que les épidémies récentes dans ces trois pays ont toutes eu lieu en milieu urbain, dans des villes importantes situées à proximité de vastes plans d’eau. Les auteurs font également ressortir que ces villes sont localisées le long de corridors utilisés par les oiseaux migrateurs14,18,19. Pour Hubalek20, l’apparition d’épidémies est associée à des facteurs favorisant l’augmentation de la densité des moustiques vecteurs, comme l’irrigation, les fortes pluies suivies d’inondations puis de températures sèches et chaudes, et la formation d’habitats favorables à la reproduction des moustiques. Les éclosions urbaines associées au Culex pipiens toucheraient un plus grand nombre de personnes20.
Les épidémies européennes semblent partager certaines caractéristiques. En effet, elles sont maximales la première année, suivies de quelques cas d’infections humaines lors des seconde et troisième années et exceptionnellement, lors d’une quatrième année20. En Europe, le caractère pathogène des épidémies est variable. Certaines épidémies n’ont touché que les animaux, d’autres que les humains et d’autres encore, les animaux et les humains3.
Avant 1990, les épidémies humaines d'infection par le VNO étaient considérées peu sévères n'entraînant que peu ou pas de décès. Cependant, les récentes épidémies de Roumanie, de Russie, d’Israël et des États-Unis se caractérisent par un taux de mortalité relativement élevé (5 à 14 %) chez les personnes présentant des symptômes neurologiques14,18,19,21. De plus, certains aspects cliniques diffèrent des éclosions antérieures, notamment la présence de faiblesse musculaire et l’augmentation du nombre de cas humains sévères. Pour ces raisons, plusieurs auteurs posent l’hypothèse que le pouvoir pathogène du virus puisse s’être modifié depuis quelques années3,11,19,21,22. D’autres sont d’avis que ces changements sont plutôt dus à l’amélioration de la surveillance hospitalière exercée16.
Soulignons que le nombre élevé de cas en Roumanie, lors de l’épidémie de Bucarest, s’explique en partie par les conditions de vie des habitants qui cohabitaient dans leur domicile avec des densités élevées de moustiques vecteurs23. En Russie, l’épidémie de Volgograd a touché un nombre impressionnant de personnes, incluant plusieurs cas de syndromes cliniques moins sévères19.
Cependant, l’épidémie d’Israël en 2000, avec son haut taux de cas humains sévères et sa létalité importante tant chez les humains (14 % parmi les cas hospitalisés) que chez les oiseaux, semble appuyer l’hypothèse de l’apparition d’une souche plus virulente. Rappelons que dans ce pays, le VNO est considéré comme endémique et la population comme largement immunisée11,21.
L’épidémie de New York
Impact sur la santé humaine
En Amérique du Nord, le VNO a fait son apparition à New York en 1999. Le tableau 2 présente les caractéristiques épidémiologiques des épidémies survenues à cet endroit en 1999 et 200014-17,29.
Tableau 2. Caractéristiques des épidémies d’infection au VNO survenues aux États-Unis en 1999 et 2000
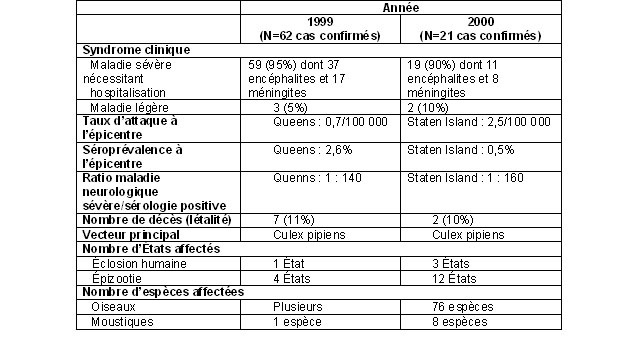
L’identification de 62 cas symptomatiques confirmés en 1999 contre 21 cas en 2000 suggère qu’il y a eu approximativement trois fois moins d’infections en 2000 malgré une augmentation du nombre d’États touchés par la présence du VNO chez les animaux. Bien que cette diminution des infections ait pu être en partie attribuable au contrôle vectoriel, d’autres activités de prévention de même que la nature sporadique et variable des épidémies au VNO peuvent aussi en être responsables11. D’ailleurs, l’expérience européenne démontre que l’incidence de la maladie humaine est maximale au cours de la première année et diminue au cours des années suivantes20.
Les indicateurs de l’activité du VNO
À la suite de l’épidémie de 1999, les organismes américains de santé publique ont commencé à utiliser les corneilles retrouvées mortes comme événement sentinelle. Le «dead crow density factor» a été proposé comme indicateur précoce étant donné qu’il semblait y avoir une corrélation entre le nombre de corneilles mortes par mille carré et le nombre de cas humains dans une région donnée30. Cependant, il est à noter que lors des épidémies de VNO sur le vieux continent, peu d’infections ni même de mortalités chez les oiseaux ont été rapportées, à l'exception d’Israël en 199828.
Aux États-Unis, en 2000, bien que les 21 personnes affectées résidaient toutes dans des comtés où des corneilles mortes ont été retrouvées, la valeur prédictive de cet indicateur demeure faible. En effet, sur 136 comtés répartis dans 12 États ayant déclaré des corneilles infectées par le VNO, seulement 10 comtés (7 %) ont rapporté au moins une personne malade31.
La corrélation entre les pools de moustiques positifs pour le VNO et la survenue de cas humains est également imparfaite. Des 21 personnes affectées, 14 résidaient dans des comtés où des pools de moustiques positifs ont été identifiés. À l’heure actuelle, le recul est insuffisant pour pouvoir juger de l’utilité d’indicateurs comme la densité de corneilles mortes et la positivité des pools de moustiques11,31.
L’utilisation d’autres oiseaux péridomestiques comme indicateur précoce est à l’étude. Komar et al.10 observent dans les comtés les plus touchés que l’oie, le poulet et le moineau ont une prévalence d’anticorps contre le VNO très élevée. Les poulets avaient aussi démontré une prévalence élevée lors de l’éclosion de 1997 en Roumanie18. D’autre part, le moineau qui combine une prévalence élevée, une compétence biologique et une grande abondance, apparaît comme un réservoir important du virus10.
L’expérience américaine nous indique que, contrairement aux encéphalites équines de l’Est et de l’Ouest qui affectent d’abord les chevaux avant d’atteindre les humains, le nombre de cas d’infections au VNO rapportés chez des chevaux a culminé après l’éclosion humaine. Il appert donc que les chevaux atteints ne puissent servir d’indicateur précoce dans l’optique d’une surveillance des cas humains12.
Autres arboviroses en Amérique du Nord
Plusieurs arboviroses sont présentes en Amérique du Nord depuis de nombreuses années. Au Québec, deux cas d’arbovirose non précisée, en 1990 et 1991, ont été déclarés au fichier provincial des maladies à déclaration obligatoire32. Aux États-Unis, les arboviroses affectant l’humain présentent des incidences et une morbidité très comparables à l’infection par le VNO33. Ainsi, l’encéphalite de Saint-Louis est largement répandue dans de nombreux États américains. Celle-ci semble être très rare au Canada : les cas rapportés dans la littérature, soit un cas au Québec en 1975 et 68 cas dans le sud de l'Ontario, semblent être reliés à l'importante épidémie d'encéphalite de Saint-Louis qui avait touché de nombreux États américains cette année-là. Tout comme l’infection par le VNO, cette maladie affecte particulièrement les personnes âgées et présente une létalité comparable.
Les arboviroses sont étroitement surveillées et étudiées depuis plus d’une vingtaine d’années aux États-Unis. Leurs cycles enzootiques sont bien connus et plusieurs éclosions, animales ou humaines, ont été bien documentées34,35.
Les épidémies associées aux virus de l’encéphalite équine de l’Ouest et de l’encéphalite de Saint-Louis sont relativement rares. Tous les cinq à dix ans, la transmission virale est plus intense et le virus s’échappe de son cycle enzootique habituel vers un cycle secondaire. Le virus infecte alors les chevaux et les humains à des niveaux épidémiques. Ce cycle secondaire de transmission du virus est complexe et difficile à initier. Plusieurs variables du cycle enzootique doivent être modifiées de façon synchrone afin que ce phénomène se produise. Parmi ces variables, mentionnons :
- l’augmentation de la population des vecteurs, déclenchée par des phénomènes météorologiques comme des pluies abondantes;
- l’amplification du virus dans les vecteurs, laquelle dépend de la température ambiante qui accélère le développement des moustiques et l’incubation virale dans les moustiques infectés;
- l’augmentation du nombre d’oiseaux infectés servant de réservoir.
Pour ces arboviroses, la surveillance du taux de séroconversion parmi les poulets sentinelles et la prévalence de la maladie chez les chevaux semblent être de bons indicateurs prédictifs de l’apparition de la maladie chez les humains33-35.
Conclusion
Identifié pour la première fois à New York en 1999, le VNO est maintenant répandu du Maine à la Floride et de la côte est vers les états du centre des États-Unis. Des oiseaux infectés ont aussi été rapportés dans le sud de l'Ontario36. Des similarités avec l’encéphalite de Saint-Louis laissent à penser que son aire de distribution pourrait s’étendre ultimement du nord de l’Argentine au sud du Canada11.
Depuis 1990, l’épidémiologie du virus semble s’être modifiée : augmentation de la fréquence d’éclosions humaines et équines; augmentation de la sévérité de la maladie chez l’humain; modification de la présentation clinique chez l’humain; présence de mortalité aviaire importante accompagnant les éclosions des États-Unis et d’Israël. Plusieurs auteurs postulent qu’il y a modification du pouvoir pathogène du virus; d’autres supposent que ces modifications s’expliquent par une meilleure surveillance hospitalière11,16. Il est difficile de prédire avec précision la survenue d’éclosions humaines d’infections dues au VNO en raison de nos connaissances partielles de l’écologie de ce virus et de la nature sporadique des épidémies humaines, du moins en Europe20,37. L’influence du réchauffement climatique sur son épidémiologie reste également à préciser38.
Aux États-Unis, un indice de mortalité aviaire a été développé dans le but de prédire la survenue de cas humains. Cet indice demeure cependant imparfait31. Des mesures de contrôle des vecteurs ont également été utilisées afin de prévenir l’apparition de cas humains (application de larvicides et d’adulticides). Cependant, l’efficacité de ces mesures reste à évaluer11.
Nos connaissances de l’écologie et de l’impact sur la santé humaine de ce virus émergent en Amérique sont en pleine évolution. Le VNO demeurera probablement une préoccupation de santé publique pour plusieurs années encore.
Références
- ANDERSON, J.F., ANDREADIS, T.G., VOSSBRINCK, C.R., TIRRELL, S., E.M. WAKEM et R.A. FRENCH, 1999. Isolation of West Nile virus from mosquitoes, crows, and a Cooper’s hawk in Connecticut, Science, 286(5448) : 2331-2332.
- LANCIOTTI, R.S., ROEHRIG J.T., DEUBEL, V., et al., 1999. Origin of the West Nile virus responsible for an outbreak of encephalitis in the northeastern United States, Science, 286(5448) : 2333-2337.
- ZELLER, H.G., 1999. West Nile : une arbovirose migrante d’actualité, Med Trop, 59(4 Pt 2) : 490-494.
- HUBALEK, Z. et J. HALOUZKA, 1999. West Nile fever – a reemerging mosquito-borne viral disease in Europe, Emerg Infect Dis, 5(5) : 643-650.
- MARTINEAU, D., 2000. Pathologie de la faune et de l’environnement. Département de microbiologie et pathologie, Faculté de médecine vétérinaire, Université de Montréal, St-Hyacinthe.
- BOURASSA, J.P., 2000. Le Moustique. Éd. du Boréal, Montréal, 244 pages.
- NASCI, R.S., SAVAGE, H.M., WHITE, D.J., MILLER, J.R., CROPP, B.C., GODSEY, M.S., KERST, A.J., BENNETT, P., K. GOTTFRIED et R.S. LANCIOTTI, 2001. West Nile virus in overwintering culex mosquitoes, New York City, 2000, Emerg Infect Dis, 7(4) : 742-744.
- ACHA, P.N. et B. SZYFRES, 1989. Zoonoses et maladies transmissibles communes à l’homme et aux animaux, 2e édition. Office international des épizooties, Paris, 1063 pages.
- GUBLER, D.J., CAMPBELL G.L., NASCI, R., et al., 2000. West Nile virus in the United States : Guidelines for detection, prevention and control, Viral Immunol, 13(4) : 469-475.
- KOMAR, N., PANELLA, N.A., BURNS, J.E., DUSZA, S.W., T.M. MASCARENHAS et T.O. TALBOT, 2001. Serologic evidence for West Nile virus infection in birds in the New York City vicinity during an outbreak in 1999, Emerg Infect Dis, 7(4) : 621-625.
- PETERSEN, L.R. et J.T. ROEHRIG, 2001. West Nile virus : a reemerging global pathogen, Emerg Infect Dis, 7(4) : 611-614.
- OSTLUND, E.N., CROM, R.L., PEDERSEN, D.D., JOHNSON, D.J., W.O. WILLIAMS et B.J. SCHMITT, 2001. Equine West Nile encephalitis, United States, Emerg Infect Dis, 7(4) : 665-669.
- RAPPOLE, J.H., S.R. DERRICKSON et Z. HUBALEK, 2000. Migratory birds and spread of West Nile virus in the western hemisphere, Emerg Infect Dis, 6(4) : 319-328.
- NEW YORK CITY, 2001. West Nile virus surveillance and control : An update for healthcare providers in New York City, City Health Information, 20(2) : 1-8.
- CENTERS FOR DISEASE CONTROL AND PREVENTION, 2001. Serosurveys for West Nile virus infection - New York and Connecticut counties, 2000, MMWR, 50(3) : 37-39.
- MOSTASHARI, F., BUNNING, M.L., KITSUTANI, P.T., SINGER, D.A., NASH, D., COOPER, M.J., KATZ, N., LILJEBJELKE, K.A., BIGGERSTAFF, B.J., FINE, A.D., LAYTON, M.C., MULLIN, S.M., JOHNSON, A.J., MARTIN, D.A., E.B. HAYES et G.L. CAMPBELL, 2001. Epidemic West Nile encephalitis, New York, 1999 : results of a household-based seroepidemiological survey, Lancet, 358 : 261-264.
- NASH, D., MOSTASHARI, F., FINE, A., MILLER, J., O’LAERY, D., MURRAY K., et al., 2001. The outbreak of West Nile virus infection in the New York City area in 1999, New Engl J Med, 344(24): 1807-1814.
- CERNESCU, C., NEDELCU, N.I., TARDEI, G., S. RUTA et T.F. TSAI, 2000. Continued transmission of West Nile virus to humans in southeastern Romania, 1997-1998, J Infect Dis, 181(2) : 710-712.
- PLATONOV, A.E., SHIPULIN, G.A., SHIPULINA O.Y., TYUTYUNNIK, E.N., FROLOCHKINA, T.I., LANCIOTTI, R.S., YAZYSHIN, A,S., PLATONOVA, O.V., OBUKHOV, I.L., ZHUKOV, A.N., Y.Y. VENGEROV et V.I. POKROVSKII, 2001. Outbreak of West Nile virus infection, Volgograd region, Russia 1999, Emerg Infect Dis, 7(1) : 128-132.
- HUBALEK, Z., 2000. European experience with the West Nile virus ecology and epidemiology: could it be relevant for the New World? Viral Immunol, 13(4) : 415-426.
- WEINBERGER, M., PITLIK, S.D., GANDACU, D., LANG, R., NASSAR, F., BEN DAVID, D., RUBINSTEIN, E., IZTHAKI, A., MISHAL, J., KITZES, R., SIEGMAN-IGRA, Y., GILADI, M., PICK, N., MENDELSON, E., BIN, H., T. SHOHAT et M.Y. CHOWERS, 2001. West Nile fever outbreak, Israel 2000 : epidemiologic aspects, Emerg Infect Dis, 7(4) : 686-691.
- CHOWERS, M.I, LANG, R., NASSAR, F., BEN-DAVID, D., GILADI, M., RUBINSTEIN, E., MISHAL, A., SIEGMAN-IGRA, A., KITZES, R., PICK, N., LANDAU, Z., WOLF, D., BIN, H., MENDELSON, E., S.D. PITLIK et M. WEINBERGER, 2001. Clinical characteristics of the West Nile fever outbreak, Israel, 2000, Emerg Infect Dis, 7(4) : 675-678.
- HAN, L.L., POPOVICI, F., ALEXANDER, J.P., et al., 1999. Risk factors for West Nile virus infection and meningoencephalitis, Romania, 1996, J Infect Dis, 179(1) : 230-233.
- PANTHIER, R., HANNOUN, C., D. BEYTOUT et J. MOUCHET, 1968. Épidémiologie du virus West Nile : étude d’un foyer en Camargue. Les maladies humaines, Ann Inst Pasteur, 115 : 435-445.
- MCINTOSH, B.M., JUPP, P.G., I. DOS SANTOS et G.M. MEENHENAN, 1976. Epidemics of West Nile and Sindbis viruses in South Africa with Culex (Culex) univittatus Theobald as vector, South African J Science, 72 : 295-300.
- LE GUENNO, B., BOUGERMOUH, A., T. AZZAM et R. BOUAKAZ, 1996. West Nile: a deadly virus? Lancet, 348(9037) : 1315.
- TSAI, T.F., POPOVICI, F., CERNESCU, C., G.L. CAMPBELL et N.I. NEDELCU, 1998. West Nile encephalitis epidemic in southeastern Romania, Lancet, 352(9130): 767-771.
- SIEGEL-ITZKOVICH, J., 2000. Twelve die of West Nile Virus in Israel, BMJ, 321(7263): 724.
- CENTERS FOR DISEASE CONTROL AND PREVENTION, 1999. Outbreak of West Nile-like viral encephalitis-New York, 1999, MMWR, 48(38) : 845-849.
- EIDSON, M., MILLER, J., KRAMER, L., B. CHERRY et Y. HAGIWARA, 2001. Dead crow densities and human cases of West Nile virus, New York State, 2000, Emerg Infect Dis, 7(4) : 662-664.
- MARFIN, A.A., PETERSEN, L.R., EIDSON, M., MILLER, J., HADLER, J., FARELLO, C., WERNER, B., CAMPBELL, G.L., LAYTON, M., SMITH, P., BRESNITZ, E., et the arboNET Cooperative Surveillance Group, 2001. Widespread West Nile activity, Eastern United States, 2000, Emerg Infect Dis, 7(4) : 730-735.
- LOUCHINI, R., 2001. Surveillance des maladies infectieuses et des intoxications chimiques à déclaration obligatoire au Québec, de 1990 à 1999. MSSS, Québec, 280 pages.
- CALISHER, C.H., 1994. Medically important arboviruses of the United States and Canada, Clin Microbiol Rev, 7(1) : 89-116.
- CENTERS FOR DISEASE CONTROL AND PREVENTION, 1988. Current Trends Arboviral Infections of the Central Nervous System - United States, 1987, MMWR, 37(33): 506-508, 513-515
- MEEHAN, P.J., WELLS, D.L., PAUL, W., BUFF, E., LEWIS, A., MUTH, D., HOPKINS, R., N. KARABASTOS et T.F. TSAI, 2000. Epidemiological features of and public health response to a St-Louis encephalitis epidemic in Florida, 1990-1, Epidemiol Infect, 125: 181-188.
- Bureau de surveillance épidémiologique, 2001. Virus du Nil occidental. Flash VNO, 2(10): 1-5.
- DAY, J.F., 2001. Predicting St-Louis encephalitis virus epidemics : lessons of recent, and not so recent, outbreaks, Ann Rev Entomol, 46 : 111-138.
- REEVES, W.C., HARDY, J.L., W.K. REISEN et M.M. MILBY, 1994. Potential effect of global warming on mosquito-borne arboviruses, J Med Entomol, 31(3): 323-332.

