Étude sur les risques associés à la contamination chimique des mollusques
De nombreux résidents de la Côte-Nord du Saint-Laurent s’adonnent à la récolte de mollusques à des fins de consommation personnelle. Cette activité entraîne une exposition à différents contaminants présents dans ces organismes. Le Programme canadien de contrôle sanitaire des mollusques, actuellement en place, a pour rôle d’exercer un suivi régulier de la qualité des mollusques récoltés de façon artisanale. Le programme est mis en œuvre conjointement par Environnement Canada, l’Agence canadienne d’inspection des aliments et le ministère des Pêches et Océans. Environnement Canada et l’Agence canadienne d'inspection des aliments sont responsables de la surveillance régulière de la qualité bactériologique de l’eau et des concentrations de toxines dans les mollusques alors que le rôle du ministère des Pêches et Océans consiste, entre autres, à ouvrir ou à fermer les secteurs de récolte en fonction des recommandations de ces deux organismes1.La contamination par les substances chimiques est exclue du programme actuel de contrôle.
L’étude faisant l’objet du présent article consistait à: documenter avec le plus de précision possible la consommation de mollusques chez les cueilleurs de la région de la Côte-Nord; analyser des échantillons de mollusques de la région concernée afin de déterminer la nature des contaminants ainsi que leurs teneurs en contaminants chimiques et évaluer le risque chimique (cancérogène et non-cancérogène) associé à cette consommation.
Aspects méthodologiques
Population à l’étude
La population à l’étude était constituée de cueilleurs de mollusques résidant sur la Haute-Côte-Nord, plus précisément dans la zone côtière située entre Tadoussac et Baie-Trinité. Dix-huit secteurs de récolte fréquemment visités ont été identifiés. La population totale de cette région était de 48 000 habitants en 2001.
Évaluation des habitudes de consommation
Deux méthodes ont servi à estimer la consommation de mollusques. La première consistait à rencontrer directement les cueilleurs de mollusques au moment où ils pratiquaient leur activité. Lors de ces rencontres, des entrevues semi-dirigées se sont déroulées selon une approche validée2-4. Chaque entrevue, d’une durée approximative de 15 minutes, comportait des questions sur la fréquence de la récolte, sur l’expérience que les cueilleurs avaient de l’activité, sur les espèces récoltées ainsi que sur le nombre hebdomadaire de repas de ces mollusques au cours de l’année précédant l’enquête. Les sites répertoriés ont été visités à deux reprises dans le but de maximiser le nombre d'entrevues. La deuxième méthode utilisée consistait à faire compléter, par les participants rencontrés, dès la première fois, un journal alimentaire couvrant une période de 30 jours. La consommation de mollusques devait être décrite avec précision, soit le nombre de repas de mollusques, la date de ces repas, le type et la provenance des mollusques ainsi que les quantités consommées.
Territoire d’échantillonnage et analyses de laboratoire
Parmi les 18 secteurs coquilliers initialement sélectionnés, huit ont été retenus pour les fins de l’analyse chimique des mollusques. La sélection a été réalisée sur la base de la présence des cueilleurs ainsi que de celle de sources de pollution chimique (dépotoirs, eaux usées, scieries, etc.).L’échantillonnage s’est déroulé au printemps 1997.Dans chacun des secteurs d’échantillonnage, un nombre suffisant de spécimens a été obtenu pour la préparation de trois homogénats de 200 g de chair chacun (30 spécimens par homogénat).Les contaminants ont été sélectionnés sur la base de leur propriété de bioaccumulation dans les invertébrés marins et en raison des effets suspectés ou reconnus sur la santé humaine. Dix métaux et métalloïdes (arsenic, mercure, sélénium, cadmium, nickel, zinc, chrome, plomb, cuivre, manganèse), 22 hydrocarbures aromatiques polycycliques (HAPs), 14 congénères de biphényles polychlorés (BPC) et 10 pesticides chlorés ont ainsi été analysés. Il est à noter que plusieurs formes d’arsenic ont été analysées soit: l’arsenic trivalent (As+3), l’arsenic pentavalent (As+5), l’acide diméthylarsinique (ADMA), le monométhylarsonique (AMMA) ainsi que l’arsenobétaïne et l’arsénocholine, deux formes d’arsenic alimentaire retrouvés surtout dans les poissons, les mollusques et les crustacés. L'ensemble des analyses chimiques a été réalisé par le laboratoire de la Direction de la toxicologie humaine de l'Institut national de santé publique du Québec (laboratoire certifié ISO 17025 par le Standards Council of Canada).Dans le cas où la concentration d’un contaminant était plus faible que le seuil de détection, on utilisait la moitié de ce seuil dans le calcul de la concentration moyenne.
Estimation de l’apport en contaminants
L’apport quotidien en contaminants chez un cueilleur a été estimé en multipliant le 95e percentile des concentrations de contaminants par la consommation quotidienne de mollusques, estimée lors des entrevues sur les secteurs de récolte et à partir des journaux alimentaires. Le résultat a par la suite été divisé par le poids moyen d’un adulte canadien (70 kg) afin d’obtenir l’apport en kilogramme par jour. Pour l’arsenic, le calcul était basé sur l’hypothèse que 10 % de la concentration totale contenue dans les mollusques est sous forme inorganique, tel que proposé par le Food and Drug Administration5.
Évaluation du risque
Le risque non cancérigène a été évalué pour les contaminants pour lesquels des valeurs de référence ont été proposées par le United States Environmental Protection Agency (U.S. EPA), l’Agency for Toxic Substances and Disease Registry (ATSDR), l’Organisation mondiale de la santé (OMS) ou encore Santé Canada. En ce qui a trait au risque de cancer, il a été évalué pour les substances de catégorie A (cancérigènes chez l’humain) et de catégories B1 et B2 (cancérigènes probables chez l’humain), tel que défini par le U.S. EPA6 et pour lesquelles un coefficient de cancérogénicité (indice de pente dose/effet) est disponible pour l’exposition par voie orale. Seuls les contaminants présents dans au moins 70 % des homogénats ont été conservés pour les deux catégories de risque.
Résultats
Habitudes de consommation
Au total, 162 participants ont collaboré à l’étude. Les principaux résultats concernant les caractéristiques des cueilleurs et leurs habitudes de consommation de mollusques sont présentés au tableau 1.
Tableau 1. Caractéristiques des cueilleurs et de leurs habitudes de consommation
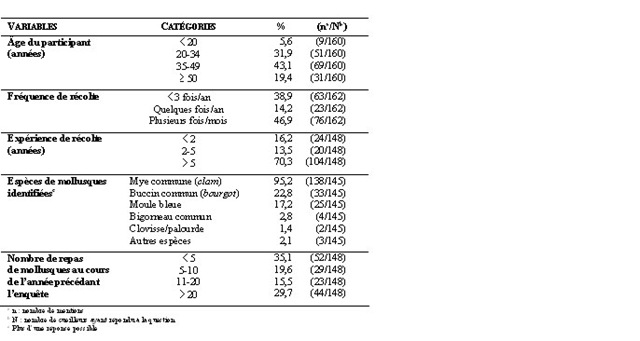
Parmi ces participants, 24 ont complété et retourné le journal alimentaire. Ces données ont permis de documenter 90 repas, la plupart (65,6 %) étant constitué de myes. Au cours d’un repas moyen, les cueilleurs consomment 47 mollusques, soit environ 410 g de chair (le poids d’une mye étant estimé à 8,7 g). Quatre scénarios de consommation ont été élaborés, les deux premiers à partir des données de la présente étude et les deux autres, en utilisant des données de consommation tirées de la littérature.
Le premier scénario est basé sur la consommation moyenne de mollusques lors d’un repas (410 g) et sur la fréquence annuelle moyenne calculée de 15 repas, totalisant 6,2 kg par année ou 17 g par jour. Le deuxième scénario représente les consommateurs réguliers. Il est basé sur une consommation annuelle de 35 repas (médiane chez les consommateurs de 20 repas et plus) et s’applique à 30 % de la population à l’étude. Sur une base annuelle, la consommation estimée s’élève à 14,6 kg, soit une consommation quotidienne de 40 g. Le troisième scénario illustre la consommation chez les consommateurs réguliers, dans un contexte d’abondance et d’accessibilité de la ressource. Il a été assumé que ce type de consommateurs remplaçait un jour sur deux la quantité moyenne de viande et de volaille consommée (estimée à 112 g/j par Statistiques Canada7) par des mollusques. La quantité de mollusques associée à ce scénario est donc de 56 g par jour ou 56 repas par année. Le dernier scénario représente une estimation basée sur le 95e percentile de consommation quotidienne de mollusques mesurée au Royaume-Uni8, une consommation évaluée à 95 g par jour ou 85 repas par année.
Contamination
Trente-six des 56 contaminants sélectionnés ont été détectés dans les homogénats (tableaux 2 et 3). Les résultats sont disponibles pour 23 homogénats au lieu des 24 prévus puisque dans un des secteurs, le nombre de spécimens échantillonnés n’a permis la préparation que de deux des trois homogénats prévus au devis d’étude. Par ailleurs, seuls les résultats obtenus pour les myes sont présentés compte tenu de leur popularité. Les résultats sont exprimés en poids humide, la proportion en eau étant de 88,4 %. L’ensemble des métaux a été détecté dans les 23 homogénats analysés. La spéciation de l’arsenic révèle que 8,2 % de la concentration totale est sous forme inorganique (étendue : 1,8 %-19 %). Parmi les composés organiques, les congénères de BPC (no IUPAC 138, 153 et 187), le naphtalène, l’hexachlorobenzène, le p,p’-dichlorodiphényle-trichloroéthane (p,p’-DDT) et le p,p’-dichloro-diphényldochloroéthylène (p,p’-DDE) ont été détectés dans tous les homogénats.
Risques chimiques
L’apport en contaminants associé à chacun des quatre scénarios est présenté au tableau 2 et se base sur l’hypothèse que les mollusques consommés sont des myes. Aucun des apports en contaminants n’excède les recommandations d’exposition les plus conservatrices pour les effets non-cancérogènes. Le risque de cancer a été évalué pour les BPC, le chlordane, l’hexachlorobenzène, l’arsenic inorganique, le p,p’-DDE et le p,p’-DDT.
Tableau 2. Apport en contaminants (mg/kg/j) associé aux différents scénarios de consommation
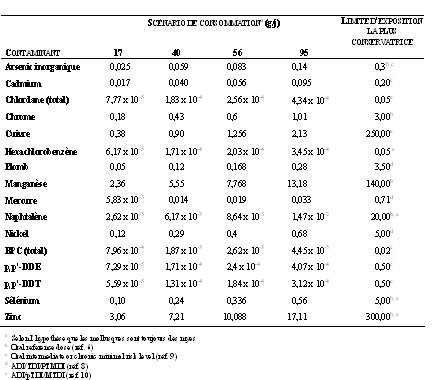
Le risque de cancer est plus élevé que 1 x 10-6 pour les BPC et plus élevé que 1 x 10-5 pour l’arsenic inorganique et ce, dès le premier scénario de consommation, soit à partir de 17 g par jour (tableau 3).
Tableau 3 : Risque de cancer au cours d’une vie associé aux différents scénarios de consommation
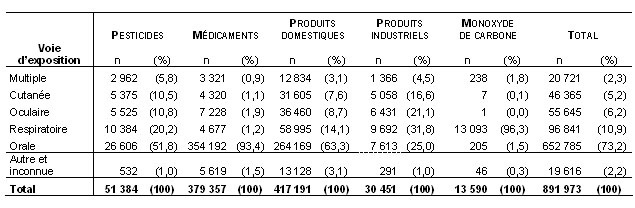
Discussion
Les résultats de la présente étude suggèrent que la consommation de mollusques récoltés sur la Côte-Nord n’entraîne pas de risque d’effet non-cancérogène pour le consommateur. Cette observation doit toutefois être nuancée par plusieurs considérations méthodologiques. En premier lieu, l’étude ne couvre pas tous les secteurs coquilliers et le nombre total d’échantillons est faible. Par ailleurs, pour certains scénarios de consommation, l’exposition la plus élevée se situe près de la limite d’exposition la plus conservatrice disponible (par exemple, pour l’arsenic inorganique, le cadmium et le chrome). Troisièmement, les limites d’exposition recommandées par les divers organismes ne sont pas nécessairement conservatrices11. De plus, l’utilisation du poids d’un adulte de 70 kg dans l’estimation de l’apport en contaminants sous-estime le risque pour les enfants, puisque ces derniers consomment trois ou quatre fois plus de nourriture que les adultes en proportion de leur poids, absorbant ainsi une plus grande quantité de contaminants par unité de masse corporelle12. Finalement, il n’existe pas de « seuil sans effet » pour certains contaminants (le plomb, par exemple).
En ce qui concerne les effets cancérogènes, l’évaluation du risque était de 1 x 10-5 et ce, même pour le scénario de la plus faible consommation (17 g/j). Dans ses recommandations concernant la consommation de poisson, le U.S. EPA13 vise à maintenir le risque de cancer à moins de 1 x 10-5. Nos résultats indiquent ainsi un risque élevé de cancer associé à la consommation de myes au sein des secteurs étudiés.
Les fruits de mer sont reconnus comme l’une des principales sources alimentaires d’arsenic14,15. Cependant, l’arsenic présent dans les mollusques est généralement sous forme organique, considérée non toxique, contrairement aux formes inorganiques, telles l’arsenic trivalent (As+3) et l’arsenic pentavalent (As+5). Aussi, bien que les formes d’arsenic trouvées en plus grande quantité dans ces organismes soient l’arsenobétaïne et les sucres arsénicaux16, nous avons constaté que les mollusques pouvaient contenir une proportion non négligeable d’arsenic inorganique (jusqu’à 19 % dans un des homogénats), proportion s’accroissant avec le niveau de contamination environnementale.
La proportion moyenne d’arsenic inorganique mesurée dans notre étude étant comparable à celle rapportée par le FDA (10 %), nous avons utilisé cette dernière dans nos calculs d’apport alimentaire, puisque jugée moins sujette à l’erreur expérimentale.
L’arsenic inorganique a été identifié comme un cancérogène du groupe A par le U.S. EPA. De nombreuses études épidémiologiques ont démontré que l’ingestion d’arsenic inorganique lors de la consommation d’eau potable accroît l’incidence du cancer de la peau, de la vessie et du poumon, les deux derniers types étant considérés comme la principale source de préoccupation17. L’arsenic inorganique présent dans les mollusques représente ainsi un risque potentiel pour la santé des cueilleurs.
Il n’existe aucun consensus scientifique sur la quantité d’arsenic inorganique absorbé par l’organisme après un repas de fruits de mer. Dans leur étude, Buchet et al.18 concluent que la quantité absorbée n’est pas biologiquement significative. Cependant, d’après les résultats de cette même étude, l’excrétion d’arsenic inorganique chez des consommateurs réguliers de fruits de mer était plus élevée (p < 0,05) par rapport à ceux qui ne consomment jamais ces aliments.
Alors que le caractère non toxique de l’arsenobétaïne excrété rapidement sans être métabolisé a été démontré à plusieurs reprises19, les effets des sucres arsénicaux sont encore peu connus. De fait, de récentes études ont démontré dans l’urine d’individus ayant consommé des sucres arsénicaux la présence de ADMA, de diméthylarsinoéthanol, d’oxyde de triméthylarsine et de nombreux métabolites dont la nature et la toxicité sont encore inconnus20,21. Ces résultats révèlent que les sucres arsénicaux, qui sont l’une des plus importantes formes d’arsenic présentes dans les mollusques16, sont non seulement biotransformés après leur ingestion, mais pourraient aussi posséder un potentiel toxique. De plus, les pouvoirs cytotoxiques et génotoxiques importants des métabolites intermédiaires trivalents produits lors de la formation du ADMA et de l’oxyde de triméthylarsine à partir de l’arsenic inorganique ont été récemment démontrés22,23. La démonstration du potentiel toxique de d’autres formes d’arsenic présentes dans les invertébrés marins représente une nouvelle considération dont il faudra tenir compte dans l’avenir.
Le risque de cancer associé à l’arsenic inorganique a été estimé dans notre étude en utilisant le coefficient de cancérogénicité proposé dans la banque de données IRIS6. Il est à noter que le modèle dose-réponse utilisé par le U.S. EPA fournit un estimé de risque plus faible que celui développé par le NRC17.
Les BPC (exprimés en Aroclor) présents dans les mollusques ont été associés, dans notre étude, à un risque de cancer supérieur à 1 x 10-6. Les résultats de l’analyse des BPC ont été exprimés sous forme d’Aroclor 1260, une méthode d’approximation de tous les congénères de BPC24. Pour les échantillons de faible niveau trophique, tels que les myes et les moules, cette méthode s’est avérée équivalente à un modèle qui utilise les données de l’ensemble des congénères25. Les BPC sont classés comme un cancérogène du groupe 2B6. Le mirex, le lindane et la plupart des HAPs n’ont pas été détectés dans nos homogénats. Ces résultats ne signifient pas pour autant que ces substances ne sont pas présentes dans l’environnement. Ceci soulève la question de la limite de détection ainsi que les conséquences d’une évaluation du risque limitée aux contaminants détectés dans une certaine proportion d’échantillons (70 % dans le cas présent). À titre d’exemple, si tous les homogénats contenaient du benzo(a)pyrène à des concentrations situées légèrement sous la limite de détection de 1 µg/kg, le risque de cancer associé serait d’environ 1,77 x 10-6 pour un apport quotidien de 95 g. Ceci fait ressortir qu’une limite de détection relativement élevée pourrait conduire à une sous-estimation du risque de cancer. D'un autre côté, le fait de considérer les contaminants indépendamment de leur fréquence de détection entraînerait une estimation du risque non réaliste.
Il est à noter que certains types de mollusques considérés dans cette étude ont des concentrations en arsenic et en BPC plus élevées (moules bleues) ou égales (palourdes)(données non présentées) à celles mesurées dans les myes. Ainsi, selon le type de mollusques consommé, les risques de cancer pourraient différer de ceux que nous avons évalués.
Au cours de notre étude, l’évaluation des effets sur la santé pour chacun des contaminants a été réalisée de manière indépendante. Il est particulièrement intéressant de noter que les deux contaminants qui sont associés à un risque élevé de cancer, ont des modes d’action complémentaires. Le mode d’action spécifique de l’arsenic dans l’induction du cancer n’a pas été établi avec certitude, mais les études suggèrent que l’arsenic pourrait agir comme cocarcinogène lors des phases de promotion et de progression17. Les BPC, quant à eux, induisent des tumeurs par des modes d’action qui n’impliquent pas la mutation des gènes6. Il est ainsi possible que le risque de cancer calculé ici sous-estime le risque associé au mélange de contaminants. Toutefois, notre évaluation du risque pourrait aussi surestimer le risque réel en présence d’une interaction neutralisante. Par exemple, il est possible que le sélénium, présent dans les mollusques, possède une action protectrice contre les effets génotoxiques de l’arsenite de sodium26.
De la même façon, l’absorption de contaminants combinée aux habitudes de vie pourraient mener à un accroissement important du risque de cancer. Mentionnons par exemple que la consommation d’eau contenant de l’arsenic inorganique jumelée à l’inhalation de fumée de cigarette entraînent chez les fumeurs un risque beaucoup plus élevé de développer un cancer du poumon que celui prédit par un modèle additif impliquant ces deux substances27,28.
De manière générale, nous considérons que notre évaluation du risque est basée sur des scénarios valides. Étant donné que la consommation moyenne de mollusques observée au Royaume-Uni8 varie entre 13,0 et 18,9 g/j, notre premier scénario (17 g/j) semble bien refléter le scénario du consommateur moyen. Le deuxième scénario (40 g/j) nous apparaît réaliste puisqu’il est comparable au 90e percentile (36,4 g/j) de l’étude menée au Royaume-Uni8.Le troisième scénario basé sur une consommation quotidienne de 56 g est tout à fait comparable à la consommation quotidienne de fruits de mer mesurée lors d’une étude menée chez les pêcheurs commerciaux du territoire29. Finalement, le dernier scénario (95 g/j) est du même ordre de grandeur que la valeur recommandée pour caractériser une consommation maximale chez des personnes qui vivent des produits de leur pêche (165 g/j)30.
Avec une consommation individuelle quotidienne évaluée à 17 g, comparée à 3,81 g pour la population canadienne7, on constate que la population de l’étude a un caractère particulier, mais probablement non unique au pays.
Conclusion
Dans cette étude, aucun des contaminants observés dans les mollusques ne représente un apport excédant les valeurs de référence recommandées pour les effets non cancérogènes. Sur ce point toutefois, certaines limites doivent être considérées avant de tirer une conclusion définitive. Des risques de cancer supérieurs à 1 x 10-5 et pouvant même excéder 1 x 10-4 ont toutefois été mesurés. Des études supplémentaires sont nécessaires afin d’améliorer la compréhension de la toxicocinétique de l’arsenic contenus dans les mollusques. La prise d’échantillons biologiques chez quelques cueilleurs de mollusque pourrait être une option envisagée. Compte tenu des résultats de notre étude, l’implantation d’un programme de surveillance de la contamination chimique des mollusques récoltés sur une base récréative est fortement recommandée. Un tel programme pourrait conduire par la suite à l’élaboration d’un guide de consommation des mollusques.
Références
- Pêches et Océans Canada (MPO) 2002. Fiche d’information Fermeture de secteurs coquilliers, (FI-MAR-02)
- LaRue A, Grondin J, Lévesque B, LaRue R, Boudreault D. 1996. La baignade dans le secteur d’eau douce du Saint-Laurent: Discours et pratiques à propos des risques à la santé. Beauport, Québec, Canada: Unité de recherche en santé publique, Université Laval.
- LaRue R, Grondin J. 1995. Le Saint-Laurent: Les risques et les bénéfices pour la santé. Analyse des groupes de discussion. Beauport, Québec, Canada: Unité de recherche en santé publique, Université Laval.
- LaRue R, Laliberté C, Grondin J., 1996. La consommation de poisson: Le point de vue des pêcheurs sportifs. Bulletin d’information en santé environnementale. 7:4-5.
- FDA 1993. Guidance for Arsenic in Shellfish. Washington, DC: Center for Food Safety and Applied Nutrition, U.S. Food and Drug Administration
- U. S. EPA 2003. Integrated Risk Information System (IRIS). Washington, DC: U.S. Environmental Protection Agency. Disponible: www.epa.gov/iris [consultée le août 2003].
- Statistiques Canada 2003. Food Statistics 2(2). Ottawa, Ontario, Canada. Disponible: www.statcan.ca/english/freepub/21-020-XIE/free.htm [consultée le 15 août 2003].
- WHO 1985 Guidelines for the Study of Dietary Intakes of Chemical Contaminants. Offset Publication No. 87. Geneva, Switzerland: Global Environmental Monitoring System.
- ATSDR 2003 Toxicological Profile Information Sheet. Atlanta, GA: Agency for Toxic Substances and Disease Registry. Disponible: www.atsdr.cdc.gov/toxpro2.html [consultée le 15 août 2003].
- Santé et Bien-Être Canada 1985. Ligne directrices sur les contaminants chimiques du poisson et des produits du poisson au Canada. Ottawa, Ontario, Canada : Loi et Règlement des Aliments et drogues.
- Hattis D, Baird S, Goble R 2002. A straw man proposal for a quantitative definition of the RfD. Drug Chem Toxicol 25:403-36.
- U.S. EPA 2003. Children’s Environmental Exposures. Atlanta, GA. Disponible: www.yosemite.epa.gov/ochp/ochpweb.nsf/content/3_Intro.htm [consultée le 26 février 2004].
- U.S. EPA 1999 Polychlorinated Biphenyls (PCBs) Update Impact on Fish Advisories, Fact Sheet. Washington, D.C., U.S. Environmental Protection Agency. Office of Water. Disponible: www.epa.gov/waterscience/fish/pcb.pdf [consultée le 4 mai 2004].
- Muñoz O, Devesa V, Suñer MA, Vélez D, Montoro R, Urieta I et al. 2000. Total and inorganic arsenic in fresh and processed fish products. J Agric Food Chem 48:4369-4376.
- Suñer MA, Devesa V, Muñoz O, LMòpez F, Montoro R, Arias AM et al. 1999 Total and inorganic arsenic in the fauna of the Guadalquivir estuary: environmental and human health implications. Sci Total Environ 242:261-270.
- Li W, Wei C, Zhang C, van Hulle M, Cornelis R, Zhang X 2003. A survey of arsenic species in Chinese seafood. Food Chem Toxicol 41:1103-10.
- National Research Council 2001. Arsenic in Drinking Water: 2001 Update. Washington DC; National Academy Press.
- Buchet, Jp, Lison, D., Ruggeri, M., Foa, V., Elia, G. 1996 Assessment of exposure to inorganic arsenic, a human carcinogene, due to the consumption of seafood. Arch Toxicol 70:773-778
- Sabbioni E, Fischback M, Pozzi G, Pietra R, Gallorini M, Piette JL. 1991. Cellular retention, toxicity and carcinogenic potential of seafood arsenic. I. Lack of cytotoxicity and transforming activity of arsenobetaine in the BALB/3T3 cell line [Abstract]. Carcinogenesis 12:1287-1291.
- Francesconi KA, Tanggaard R, McKenzie DJ, Goessler W. 2002. Arsenic metabolites in human urine after ingestion of an arsenosugar. Clin Chem 48:92-101.
- Le XC, Ma M, Lai V. 1999. Exposure to arsenosugars from seafood ingestion and speciation of urinary arsenic metabolites. In: Arsenic Exposure and Health Effects III (Chappell WR, Abernathy CO, Calderon RL, eds). St-Louis : Elsevier Science, 69-79.
- Mass MJ, Tennant A, Roop BC, Cullen WR, Styblo M, Thomas DJ et al. 2001. Methylated trivalent arsenic species are genotoxic. Chem Res Toxicol 14:355-361.
- Styblo M, Del Razo LM, Vega L, Germolec DR, LeCluyse EL, Hamilton GA et al. 2000. Comparative toxicity of trivalent and pentavalent inorganic and methylated arsenicals in rat and human cells. Arch Toxicol 74:289-299.
- Nadon S, Kosatsky T, Przybysz R. 2002. Contaminant exposure among women of childbearing age who eat St. Lawrence River sport fish. Arch Environ Health 57:473-81.
- Sather PJ, Newman JW, Ikonomou MG. 2003. Congener-based Aroclor quantification and speciation techniques: a comparison of the strengths, weaknesses, and proper use of two alternative approaches. Environ Sci Technol 37:5678-86.
- Biswas S, Talukder G, Sharma A. 1999. Prevention of cytotoxic effects of arsenic by short-term dietary supplementation with selenium in mice in vivo. Mutat Res 441:155-160.
- Ferreccio C, Gonzàlez C, Milosavjlevic V, Marshall G, Sancha AM, Smith AH. 2000. Lung cancer and arsenic concentrations in drinking water in Chile. Epidemiology 11:673-679.
- Tsuda T, Babazono A, Yamamoto E, Kurumatani N, Mino Y, Ogawa T et al. 1995. Ingested arsenic and internal cancer: a historical cohort study followed for 33 years. Am J Epidemiol 141:198-209.
- Dewailly, É., Laliberté, C., Sauvé, L.Gingras, S. Ayotte, P. 1991. La consommation des produits de la mercure la Basse-Côte-Nord du Golfe Saint-Laurent : risques et bénéfices pour la santé, Sainte-Foy, Département de santé communautaire, Centre hospitalier de l’Université Laval.
- Cooper, CB., Doyle, ME., Kipp, K. 1991. Risks of consumption of contaminated seafood: the Quincy Bay Case Study. Environ Health Perspect 90:133-140.
Note : Adapté par Claire Laliberté à partir d’un article publié dans la revue Environmental Health Perspectives, 2004. 112(8): 883-888.
Remerciements : Pierre Ayotte pour la révision de l’analyse de risque associé aux BPC, Jean-Philippe Weber pour les analyses chimiques et Saint-Laurent Vision 2000, volet santé, pour le financement.

