Multiplier les transaminases sériques par la concentration d’acétaminophène afin de prédire la toxicité à la suite d’un surdosage
Volume 27, Numéro 1
Titre de l'article
Multiplying the serum aminotransferase by the acetaminophen concentration to predict toxicity following overdose. Clin Toxicol (Phila). 2e10 Oct;48(8):793-9.
Auteurs
Marco L.A. Sivilotti
Department of Emergency Medicine, Queen’s University, Kingston, ON, Canada
Thomas J. Green
Department of Emergency Medicine, Queen’s University, Kingston, ON, Canada
Caillin Langmann
Department of Emergency Medicine, Queen’s University, Kingston, ON, Canada
Mark Yarema
Department of Family Medicine, University of Calgary, Calgary, AB, Canada
Department of Physiology and Pharmacology, University of Calgary, Calgary, AB, Canada
David Juurlink
Department of Medicine, Sunnybrook Health Sciences Centre, Toronto, ON, Canada
David Johnson
Department of Pediatrics, University of Calgary, Calgary, AB, Canada
Commanditaires
- Robert and Gordon Sinclair Studentship in Biochemistry of Queen’s University;
- PSI Fondation (médecins de l’Ontario);
- Canadian Association of Emergency;
- Adult Research Committee of the Calgary Health Region;
- Cumberland Pharmaceuticals (droit illimité de subvention);
- McLaughlin Medical Education Bursary;
- JF Sparks Scholarship;
- PMAC Summer Research Program of Queen’s University;
- Alberta Heritage Foundation Studentship.
Cadre de l'étude
Cette étude descriptive est une analyse secondaire de l’étude CAOS (Canadian Acetaminophen Overdose Study), une étude multicentrique rétrospective (1980 à 2005) de cohorte de patients hospitalisés pour une intoxication à l’acétaminophène (paracétamol, APAP).
Devis
Décrire les biomarqueurs présents chez les patients qui développent une hépatotoxicité malgré un traitement à la suite d’un surdosage d’APAP. Un nouveau paramètre, soit le produit APAP x transaminases (AT), est proposé pour la stratification initiale du risque.
Patients
Les patients sélectionnés présentaient une intoxication aigüe à l ’APAP à la suite d’une ingestion unique, et ont développé une hépatotoxicité secondaire (pic sérique AST ou ALT ≥ 1000 UI/L).
Les critères d’exclusions étaient :
- Temps d’ingestion inconnu;
- Ingestions multiples sur plus de 6 heures;
- Absence de dosage de l’APAP sérique ≤ 24 heures postingestion (P-I);
- Absence de dosage des transaminases (AST, ALT) sériques > 24 heures P-I;
- Présence de lésions hépatiques préexistantes;
- Présentation tardive.
Points évalués
- Taux d’élimination de l’APAP (assumant cinétique ordre 1);
- Interdépendance de l’APAP sérique et des AT sériques;
- Utilisation de l’AT sérique ayant le plus augmenté (AST ou ALT) pour les calculs.
Résultats
Des 3 202 patients de l’étude CAOS, 94 présentaient les caractéristiques recherchées (voir figure suivante).
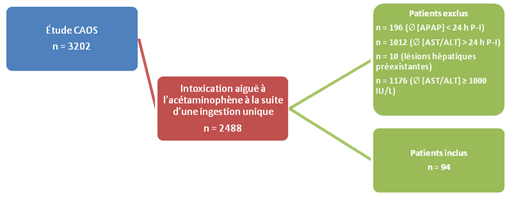
Tous les patients ont été traités avec de la NAC, initiée dans une médiane de 15,5 heures P-I. Le protocole IV de Prescott (20 h de NAC) a été utilisé dans tous les cas sauf 3 et prolongé dans le tiers des cas.
La demi-vie moyenne d’élimination de l’APAP chez les patients en surdosage était de 4,8 heures [IC 95 % : 4,4 à 5,3 heures], comparativement à la moyenne de 2 à 2,5 heures chez les patients avec une consommation normale. De plus, la demi-vie était plus longue chez les patients ayant développé des AT > 1000 UI/L au cours des 24 premières heures suivant l’ingestion (moyenne 5,7 heures).
Dans les 94 cas étudiés, les concentrations sériques d’APAP étaient encore détectables [médiane 570 µmol/L (314-983)] au moment de la première mesure des AT [211 (77-511) UI/L] à 15,3 heures (12,1-19,2) après l’ingestion, ce qui donne un produit initial APAP x AT de 99 000 (52 000 à 240 000) µmol x UI/L2. Puisque les AT s’élèvent rapidement (temps de doublement : 9,5 h) et que l’APAP s’élimine lentement (demi-vie : 4,8 h), le produit APAP x AT est demeuré élevé au cours des premières 12 à 24 heures de traitement avec la NAC, en particulier chez les patients qui ont développé une hépatotoxicité précoce.
Conclusion des auteurs
Le produit APAP x AT, calculé au moment de la présentation et après quelques heures de traitement à la NAC, semble prometteur comme nouveau prédicteur du risque à la suite d’une ingestion massive d’APAP. Il ne nécessite ni interprétation graphique, ni l’heure exacte de l’ingestion, deux limites à la stratification actuelle du risque.
Selon cette logique, chez un patient à faible risque, avec une élimination rapide d’APAP et une lente progression des AT, le produit APAP x AT diminuera rapidement. Lorsque l’élimination de l’APAP s’apparente au temps de doublement des AT (signe de mauvais pronostic), le produit APAP x AT demeurera constant dans le temps.
Discussion
Cette étude a l’avantage d’utiliser des données canadiennes, ainsi que le protocole de NAC IV le plus utilisé et le plus recommandé actuellement par nos centres antipoison.
Que pensez-vous de l’utilisation de ce paramètre (APAP x AT)? Croyez-vous qu’il pourrait vous être utile cliniquement?
Le lecteur est invité à utiliser le blogue, disponible à la suite de cet article, afin de discuter de son contenu et échanger avec d’autres professionnels.
Pour toute correspondance
Pierre-André DubéPharmacien en toxicologie clinique
Centre de toxicologie du Québec
Institut national de santé publique du Québec
945, avenue Wolfe, 4e étage, Québec (Québec) G1V 5B3
Téléphone : 418 650-5115, poste 4647
Télécopieur : 418 654-2148
Courriel : [email protected]
Dubé PA. Multiplier les transaminases sériques par la concentration d'acétaminophène afin de prédire la toxicité à la suite d'un surdosage. Bulletin d'information toxicologique 2011;27(1). [En ligne] https://www.inspq.qc.ca/toxicologie-clinique/multiplier-les-transaminas…
Bulletin d'information toxicologique, Volume 27, Numéro 1, janvier 2011
Le Bulletin d’information toxicologique (BIT) est une publication conjointe de l’équipe de toxicologie clinique de l’Institut national de santé publique du Québec (INSPQ) et du Centre antipoison du Québec (CAPQ). La reproduction est autorisée à condition d'en mentionner la source. Toute utilisation à des fins commerciales ou publicitaires est cependant strictement interdite. Les articles publiés dans ce bulletin d'information n'engagent que la responsabilité de leurs auteurs et non celle de l'INSPQ ou du CAPQ.
ISSN : 1927-0801

