État des connaissances sur la toxicité et l’exposition humaine aux phtalates
Diverses agences gouvernementales, des groupes environnementaux ainsi que le public en général sont préoccupés, depuis quelques années, par la présence de plus en plus répandue de phtalates, une famille de composés chimiques retrouvés dans les produits de consommation1-5. L’utilisation de phtalate de dibutyle, notamment dans les cosmétiques, de phtalate de di-isononyle dans les jouets et les articles de puériculture, ainsi que de phtalate de di-2-éthylhexyle dans certains dispositifs médicaux ont fait l’objet de nombreuses discussions, de rapports et d’avis de santé. Le risque lié au relargage (en très petite quantité, de façon continue) et au potentiel toxique de ces produits constitue une préoccupation pour la santé humaine. Ce texte a pour objet la révision des connaissances actuelles concernant la toxicité et l’exposition de la population aux phtalates.
Description des principaux composés de phtalates
Les phtalates font partie d’une famille de produits chimiques constitués d’un anneau benzénique et de deux groupements carboxylates générant une structure de type diester. Il s’agit de substances principalement destinées à un usage industriel. Parmi les plus couramment utilisées, mentionnons le BBP (phtalate de benzylbutyle), le DBP (phtalate de dibutyle), le DEP (phtalate de diéthyle), le DEHP (phtalate de di-2-éthylhexyle) et le DINP (phtalate de di-isononyle)2,6. On retrouve des phtalates dans plusieurs produits de consommation courante (voir tableau 1) tels les adhésifs, les revêtements de sol en vinyle, les huiles lubrifiantes, les condensateurs électriques, les détergents, les solvants, les produits pharmaceutiques, les fils et câbles électriques et les produits cosmétiques (parfums, déodorants, lotions après rasage, shampooings, aérosols pour cheveux, vernis à ongles). L’usage des phtalates comme plastifiant représente une autre des applications très courantes de ces produits. La majorité des articles rigides, semi-rigides ou souples à base de chlorure de polyvinyle, communément appelé PVC, contiennent des phtalates. La proportion de phtalates peut atteindre jusqu’à 50 % dans certains produits, notamment dans les sacs de plastiques, les cadres pour fenêtres, les emballages alimentaires, les imperméables en plastique, les rideaux de douche, les bottes, les boyaux d’arrosage, les jouets pour les enfants, les dispositifs médicaux et les contenants pour le stockage du sang.
Tableau 1. Description des principaux phtalates pour usage de type commercial et industriel 2,3,6,13
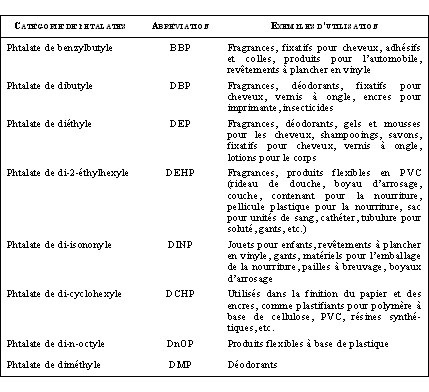
Voies d’exposition et niveaux de référence
Le contact direct avec l’air, l’eau, la nourriture ou encore les objets portés à la bouche représentent les principales voies d’exposition aux phtalates chez l’humain6. La libération des phtalates dans les divers médias est possible en raison du faible lien covalent entre ces composés et les polymères. L’ingestion d’aliments dont l’emballage contient des phtalates demeure une source importante d’exposition pour la population générale6. Selon une étude publiée en 2003, 12 % de la population générale en Allemagne excéderait la dose journalière tolérable par ingestion pour le DEHP, dose recommandée par la Communauté Européenne7 (37 mg/kg poids/jour). Les mêmes auteurs estiment que pour 31 % des individus, la consommation journalière dépasserait la dose de référence de 20 mg/kg poids/jour du Food and Drug Administration (US-FDA). L’inhalation de produits volatils présents dans certains cosmétiques (shampooings, parfums, vernis à ongles, etc.) ou même de solides comme les PVC est également une autre voie potentielle d’exposition chez les humains. L’absorption cutanée des phtalates, bien que possible, est une voie encore mal documentée. La libération de phtalates par la voie intraveineuse, lors de l’utilisation de certains dispositifs médicaux (sacs de sang, tubulures, etc.), représenterait une voie d’exposition non négligeable pour certains sous-groupes de la population6,8,9. On constate ainsi que l’usage très répandu de ces produits favorise une exposition par diverses voies chez l’humain.
Les Centers for Disease Control and Prevention (CDC) ont produit diverses publications, dont celle parue en janvier 2003, sur les niveaux de base des métabolites urinaires des phtalates retrouvés dans la population générale aux États-Unis6,8,9. Les données publiées sont tirées de l’enquête nationale de surveillance du National Health and Nutrition Examination Survey (NHANES). Les auteurs de ces rapports indiquent clairement que les concentrations urinaires des métabolites des phtalates qui sont rapportées ne signifient pas que des effets néfastes sur la santé sont nécessairement attendus à ces niveaux. Ces données permettent cependant d’établir des niveaux d’exposition de référence pour la population générale qui peuvent servir à des fins de surveillance (comparaison des niveaux et suivi temporel, par exemple). Le tableau 2 présente les principaux résultats concernant les niveaux de référence des métabolites urinaires des phtalates rapportés dans le rapport du CDC6. Les métabolites des DEP, DBP, BBP et DEHP sont les plus fréquemment détectés dans les urines6. On rapporte dans la population générale des concentrations plus élevées des métabolites urinaires du DEP, DBP et BBP par rapport aux métabolites du DEHP et du DINP, alors que ces derniers sont produits industriellement en plus grande quantité. Parmi les hypothèses avancées pour expliquer les différences observées entre les niveaux de métabolites, les auteurs mentionnent l’utilisation plus fréquente du DEP et du DBP dans les produits d’application courante qui sont facilement absorbés par inhalation, tels les cosmétiques. Ainsi, ces résultats pourraient n’être que le reflet d’une fréquence plus élevée de contact avec ce type de phtalates dans la population générale. D’ailleurs, des taux plus élevés des métabolites du DBP et du DEP ont été observés chez les femmes, notamment celles en âge de procréer6,8. L’absorption cutanée des phtalates à courtes chaînes tels le DEP, le DBP et le BBP est également une autre hypothèse avancée pour expliquer ces résultats.
Tableau 2. Concentrations urinaires (mg/L) et intervalle de confiance à 95% (IC 95%) des principaux métabolites des phtalates mesurés dans la population américaine âgée de 6 ans et plus, NHANES 1999-2000a
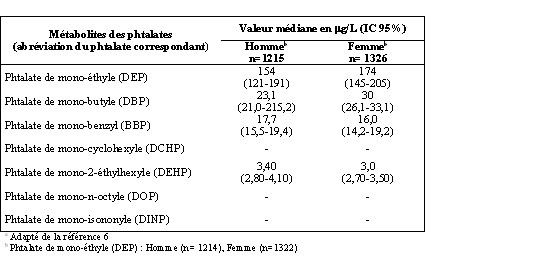
On a rapporté, dans une étude récente effectuée en Italie, la présence de DEHP et de son métabolite (MEHP) dans le plasma de femmes enceintes (n=24) et le sang au cordon ombilical des nouveau-nés. Le niveau de détection pour le MEHP chez les mères et les nouveau-nés était respectivement de 75 % et 72 %. Ces résultats suggèrent que l’exposition du fœtus aux phtalates pendant la gestation est étroitement liée à celle de la mère et qu’il y a donc transfert placentaire10. La mesure des métabolites urinaires réalisée chez 60 femmes enceintes de New York et de Cracovie11 a également révélé une exposition au DEP, DBP, BBP et DEHP à des concentrations comparables à celles rapportées dans l’enquête du NHANES de 1999-20006. Les auteurs concluent que l’inhalation de phtalates, par l’usage des produits domestiques et cosmétiques dans les maisons, est une voie significative d’exposition de la population.
Principaux effets sur la santé
Le niveau de toxicité des phtalates varie selon le type de composé. Le DEHP possède un potentiel de toxicité plus élevé que les autres phtalates6,12. Les principaux effets des phtalates rapportés dans les études expérimentales réalisées auprès de différentes espèces animales sont de l’atrophie testiculaire, une atteinte hépatique, une baisse de la fertilité, une diminution du poids fœtal, une augmentation de la masse des reins, une activité anti-androgénique ainsi que des effets tératogènes (à des doses très élevées)8,13-17. L’exposition au DEHP et au DINP a été associée à une augmentation de l’incidence d’adénome et de carcinome hépatocellulaire chez les rongeurs14,15. Une des hypothèses proposées pour expliquer ce phénomène observé chez les animaux est une prolifération des peroxysomes et des organelles cellulaires, laquelle voie métabolique ne serait pas activée chez les primates et les humains14. Plusieurs chercheurs sont cependant d’avis qu’il ne s’agit pas d’un argument suffisant pour ignorer le potentiel cancérigène des phtalates18, 19.
Chez l’humain, les effets sur la reproduction, notamment les problèmes de fertilité et le développement des nouveau-nés, sont au centre des principales préoccupations en lien avec l’exposition aux phtalates. Aux États-Unis, le Department of Health and Human Services a mis sur pied un centre d’évaluation des risques sur la reproduction humaine (The National Toxicology Program, Center for the Evaluation of Risks to Human Reproduction). Un certain nombre de phtalates a jusqu’à maintenant fait l’objet d’une évaluation par un panel d’experts afin de déterminer la toxicité de ces composés sur la reproduction et le développement. À l’exception du DEHP et du DINP et dans une moindre mesure du DBP, les experts ont conclu à des effets négligeables, sinon nuls, sur la reproduction et le développement pour la plupart des phtalates étudiés (DnOP, BBP, DIDP, DnHP)20. Néanmoins, l’usage de divers équipements médicaux suscite beaucoup d’inquiétude quant aux effets possibles du DEHP sur le développement des enfants de sexe masculin nés prématurément qui requièrent des soins prolongés. Le US-FDA ainsi que la Communauté Européenne sont également préoccupés par l’utilisation des équipements médicaux contenant du DEHP et le risque d’atteinte hépatique chez les nourrissons21,22. Par ailleurs, les études récentes qui ont évalué les effets de l’exposition aux phtalates sur la fertilité des adultes et le développement pubère des jeunes filles ne sont pas concluantes pour établir un lien de causalité12,23,24.
Mesures préventives pour diminuer l’exposition de la population
En raison de la présence de phtalates dans de nombreux produits de consommation courante, plusieurs pays, dont le Canada, ont mis de l’avant diverses mesures pour diminuer l’exposition de la population à ces substances chimiques. L’interdiction d’utiliser des phtalates dans la fabrication des jouets de dentition et les hochets pour les enfants en est un bon exemple. En 1998, à la suite d’une évaluation des risques associés aux objets contenant des DINP destinés aux enfants, Santé Canada concluait que la quantité libérée par des produits souples en PVC pouvait présenter un risque pour la santé et la sécurité des enfants âgés de 3 mois à un an25. Les fabricants, les importateurs, les distributeurs et les détaillants ont depuis lors l’obligation de s’assurer que les jouets de dentition et les hochets en plastique flexible soient exempts de DINP, de DEHP et de tous autres types de phtalates26. La Communauté Européenne a également pris des dispositions semblables pour réglementer sur l’utilisation des phtalates dans les jouets pour enfants27. D’ailleurs, au Canada et aux États-Unis, on ne retrouve plus de phtalates dans les jouets ou objets qui sont susceptibles d’être portés à la bouche par les enfants20. Toutefois, il est encore possible de retrouver des phtalates dans les jouets destinés aux enfants plus âgés, ce qui représente ainsi un risque potentiel d’exposition pour les plus petits qui partagent le même environnement. Selon les donnés du National Toxicology Program, l’exposition des enfants aux DEHP aurait déjà diminué ces dernières années, témoignant ainsi de l’efficacité des mesures entreprises aux États-Unis et au Canada20.
Plusieurs groupes environnementaux et des associations de consommateurs aux États-Unis ont dénoncé vivement la présence de phtalates dans la fabrication des cosmétiques1,3,4. Santé Canada a pour sa part produit un document d’information pour les consommateurs comportant une série de questions et réponses sur le phtalate de dibutyle (DBP) et son usage dans divers produits cosmétiques. Selon cet organisme, le DBP dans les cosmétiques ne représenterait pas de risque pour la santé lorsque la concentration est inférieure à 10 % dans le produit28. Dans le but de permettre aux consommateurs d’effectuer des choix éclairés, Santé Canada a annoncé son intention de modifier le Règlement sur les cosmétiques de manière à exiger des fabricants et des distributeurs de cosmétiques la divulgation des ingrédients sur l’étiquette de leurs produits29. En France, on s’apprête également à apporter des modifications législatives en ce sens. Tel que rapporté par l’Agence française de sécurité sanitaire des produits de santé dans son bulletin périodique d’octobre 2002, la Commission de cosmétologie a procédé à une évaluation de plusieurs phtalates et a émis plusieurs recommandations concernant la présence de ces composés dans les cosmétiques30. On y propose notamment l’interdiction d’utiliser le DEHP dans les produits cosmétiques, de restreindre l’usage du DBP et du BBP aux vernis à ongles et d’autoriser une concentration maximale de 15 % de DEP dans les produits destinés à un usage externe sur le corps et le visage, à l’exception des parfums.
Tel que mentionné précédemment, les dispositifs médicaux représentent pour la population une source non négligeable d’exposition aux phtalates, en particulier au DEHP. C’est pourquoi des solutions alternatives et des mesures de prévention devraient être mises de l’avant. On sait depuis longtemps que le DEHP peut se lessiver de la paroi intérieure des tubulures en PVC comme celles utilisées en milieu médical20,31-33. Certaines pratiques médicales présentent en effet un risque plus élevé de mobilisation du DEHP telles que : les transfusions multiples de dérivés de sang et l’oxygénation extracorporelle chez les nouveau-nés ; l’hémodialyse chez les garçons pré-pubères, les femmes enceintes ou celles qui allaitent ; les transfusions multiples de dérivés sanguins en général ; la transplantation cardiaque ou le by-pass cardio-pulmonaire ; l’alimentation parentérale (spécialement s’il s’agit de lipides dans des sacs en PVC), etc.31-33. Dans le but de protéger les groupes à risque, on devrait, dans la mesure du possible, favoriser l’usage de produits de substitution qui ne contiennent pas de DEHP lors de certaines procédures médicales prolongées. D’ici la mise en marché éventuelle de tels produits sans phtalate dans le secteur médical, il n’est pas recommandé ni même justifié pour l’instant de priver la population de certains types de traitements ou procédures puisque les bénéfices pour la santé demeurent largement supérieurs aux dangers associés à l’exposition au DEHP.
Conclusion
Chaque année, des millions de tonnes de phtalates sont produites dans le monde pour être incorporées dans une grande variété de biens de consommation courante. La présence de plus en plus répandue des phtalates dans l’environnement a incité plusieurs pays à mieux documenter l’exposition de la population6-11. Les récentes études sur le sujet semblent indiquer que les niveaux d’imprégnation aux phtalates parmi ceux les plus utilisés, comme le DINP et le DEHP, pourraient être plus importants qu’on ne le croyait7,34. En effet, l’estimation des apports quotidiens en phtalates pour certains groupes de la population serait supérieure à la dose de référence établie par divers organismes de réglementation. Toutefois, ces niveaux demeurent bien en deçà de la dose sans effet documentée dans les études expérimentales réalisées avec des animaux.
Bien que de nombreuses études aient été réalisées sur le sujet, la recherche concernant les effets des phtalates sur la santé humaine demeure incomplète et suscite encore plusieurs questions. Par exemple, le groupe d’experts-conseils canadiens sur l’évaluation du DEHP dans les dispositifs médicaux a recommandé à Santé Canada d'appuyer et de faciliter, par tous les moyens possibles, la recherche pour déterminer le niveau de risque chez les humains. Malgré cela, on ne peut espérer à court terme la mise en marché de produits de substitution, notamment pour le secteur médical, qui auraient les mêmes propriétés de résistance et de flexibilité que les phtalates. De toute façon, il sera auparavant essentiel de faire la démonstration de l’innocuité et de l’efficacité de ces produits de remplacement.
Même sans la preuve formelle que les phtalates constituent ou non un danger réel pour la santé, il est possible de poser des gestes concrets pour protéger la population. À l’instar de certains fabricants de cosmétiques, d’autres manufacturiers de produits industriels devraient également emboîter le pas dans l’application de politiques visant l’élimination des phtalates2. En attendant des réponses plus précises sur les risques à la santé associés aux phtalates, les industries et les gouvernements devraient, selon le principe de précaution, se fixer des objectifs pour limiter au maximum l’exposition de la population à ces divers composés chimiques.
Références
- DiGangi, J. et H. Norin, 2002. Pretty nasty - Phthalates in European cosmetic products. Health Care Without Harm, 25 pp.
- DiGangi, J., Schettler, T., Cobbing, M. et M. Rossi, 2002. Aggregate exposures to phthalates in Humans. Health Care Without Harm, 49 pp.
- Houlihan, J., Brody, C. et B. Schwan, 2002. Not too pretty. Phthalates, beauty products and the FDA. Environmental Working Group, Coming Clean, Health Care without Harm, 17 pp.
- Houlihan, J. et R. Wiles, 2000. Beauty secrets. Does a common chemical in nail polish pose risks to human health? Environmental Working Group, 27 pp.
- Rossi M., 2000. Neonatal exposure to DEHP and opportunities for prevention. Health Care Without Harm, 14 pp.
- U.S. Department of Health and Human Services, 2003. Second national report on human exposure to environmental chemicals. Centers for disease control and prevention, DHHS, 251 pp.
- Koch, H.M., Drexler, H. et J. Angerer, 2003. An estimation of the daily intake of di(2-ethylhexyl)phthalate (DEHP) and other phthlates in the general population. Int J Hyg Environ Health 206:77-83.
- Blount, B.C., Manori, J.S., Caudill, S.P., Needham, L.L., Pirkle, J.L., Sampson, E.J., Lucier, G.W., Jackson, R.J. et J.W. Brock, 2000. Levels of seven urinary phthalate metabolites in a human reference population. Environ Health Perspect 108(10):979-982.
- U.S. Department of Health and Human Services, 2001. National report on human exposure to environmental chemicals. Centers for disease control and prevention, DHHS, 59 pp.
- Latini, G., De Felice, C., Presta, G., Del Vecchio, A., Paris, I., Ruggieri, F. et P. Mazzeo, 2003. Exposure to Di(2-ethylhexyl)phthalate in humans during pregnancy. A preliminary report. Biology of the Neonate 83(1):22-4.
- Adibi, J.J., Perera , F.P., Jedrychowski, W., Camann, D., Barr, D., Jacek, R. et R.M. Whyatt, 2003. Prenatal exposures to phthalates among women in New York City and Krakow, Poland. Environ Health Perspect 111(14):1719-1722.
- Lovekamp-Swan, T. et B.J. Davis, 2003. Mechanisms of phthalate ester toxicity in the female reproductive system. Environ Health Perspect 111(2):139-145.
- HSDB, Hazardous Substances Data Bank. National Library of Medicine, Bethesda, Maryland (version CD-ROM), MICROMEDEX, Inc., Greenwood Village, Colorado (édition se terminant le 31 août 2003).
- IARC, 2000. Some Industrial Chemicals. IARC Monographs on the Evaluation of Carcinogenic Risks to Humans, Lyon, France. 77:41-148.
- IRIS, Integrated Risk Information System. US Environmental Protection Agency, Washington, DC (version CD-ROM), MICROMEDEX, Inc., Greenwood Village, Colorado (édition se terminant le 31 août 2003).
- IPCS, International Programme on Chemical Safety, 1992. Environmental Health Criteria 131 – Diethylhexyl phthalate, Organisation mondiale de la santé, Genève, 141 p.
- IPCS, International Program on Chemical Safety, 1997. Environmental Health Criteria 189 – Di-n-butyl phthlate, World Health Organization, Genève, 205 pp.
- Vanden Heuvel, J.P., 1999. Peroxisome proliferator-activated receptors (PPARS) and carcinogenesis. Toxicol Sci 1999 Jan;47(1):
1-8. - Melnick, R.L., 2003. Suppression of crucial information in the IARC evaluation of DEHP. Int J Occup Environ Health 9(1):84-85.
- U.S. Department of Health and Human Services, 2004. NTP-CERHR Reports and Monograph. [En ligne]. cerhr.niehs.nih.gov/reports/index.html (Série de documents sur les phtalates) (Consulté le 10 mars 2004)
- FDA, 2002. PVC devices containing the plasticizer DEHP. Public health notification. Feigal DW, Center for devices and radiological Health, Public Health Service, Department of Health & Human Services, Food an Drug Administration, 4pp.
- European Commission, 2002. Opinion on medical devices containing DEHP plasticised PVC; neonates and other groups possibly at risk from DEHP toxicity. C2-Management of scientific committees; Scientific So-operation and Networks, Directorate C – Scientific Opinions, Health and Consumer Protection Directorate-General, European Commission, 34 pp.
- Duty, S.M., Singh, N.P., Silva, M.J., Barr, D.B., Brock, J.W., Ryan, L., Herrick, R.F., Christani, D.C. et R. Hauser, 2003. The relationship between environmental exposures to phtalates and DNA damage in human sperm using the neutral comet assay. Environ Health Perspect 111(9):1164-1169.
- Colon, I., Caro, D., Bourdony, C.J. et O. Rosario, 2000. Identification of phthalate esters in the serum of young Puerto Rican girls with premature breast development. Environ Health Perspect 108(9):895-900.
- Santé Canada, 1998. Mise en garde/Avis (1998) Évaluation du risque du phtalate de di-isononyle dans les produits en vinyle pour enfants. Rapport d’enquête [En ligne]. www.hc-sc.ca/francais/protection/mises_garde/1998/risque.html
- Santé Canada, 2001. Guide des exigences canadiennes en matière de sécurité des jouets et des produits connexes dans l’industrie (suite). Programme Sécurité des produits de consommation de la sécurité des produits, Direction générale de la santé environnementale et sécurité des consommateurs, Santé Canada. [En ligne]. www.hc-sc.gc.ca/hecs-sesc/publications/jouets/considerations.htm.
- CCE (Commission des Communautés européennes), 2003. Décision de la commission du 20 mai 2003 modifiant la décision 1999/815/CE concernant des mesures qui interdisent la mise en marché de jouets et articles de puériculture destinés à être mis en bouche par des enfants de moins de trois ans, fabriqués en PVC souple contenant certains phtalates. Décision 2003/368/CE, Journal officiel de l’Union européenne.
- Santé Canada, 2003. Programme des cosmétiques. Question et réponses sur le di-butyl-phthalate (DBP). Programme de la sécurité des produits, Direction générale de la santé environnementale et sécurité des consommateurs, Santé Canada. [En ligne].www.hc-sc.gc.ca/hecs-sesc/cosmetiques/dbpqr.htm.
- Santé Canada, 2003. Programme des cosmétiques. Information - Janvier 2003. Programme de la sécurité des produits, Direction générale de la santé environnementale et sécurité des consommateurs, Santé Canada. [En ligne]. www.hc-sc.gc.ca/hecs-sesc/cosmetiques/cosmetiques.htm (consulté le 14 juillet 2003).
- Agence française de sécurité sanitaire des produits de santé, 2002. Phtalates et produits cosmétiques. Vigilances, bulletin no. 12, p. 2.
- Health Canada, 2002. Expert advisory panel on DEHP in medical devices. Final report, 22 pp.
- U.S. Food and Drug Administration, 2001. Safety assessment of di(2-ethylhexyl-phthalate (DEHP) released from PVC medical devices. Center for Devices and Radiological Health, FDA, 60 pp.
- European Commission, Health & Consumer Protection Directorate-General, 2002. Opinion on medical devices containing DEHP plasticised PVC; neonates and other groups possibility at risk from DEHP toxicity. Adopted by the Scientific committee on medicinal products and medical devices, 34 pp.
- Barr, D.B., Silva, M.J., Kato, K., Reidy, J.A., Malek, N.A., Hurtz, D., Sadowski, M., Needham, L.L. et A.M. Calafat, 2003. Assessing human exposure to phthalates using monoesters and their oxidized metabolites as biomarkers. Environ Health Perspect

